题目内容
已知葡萄糖氯化钠注射液500ml中含NaCl4.9g,葡萄糖25g,分别计算NaCl和葡萄糖的物质的量浓度.
考点:物质的量浓度的相关计算
专题:
分析:根据n=
分别计算出氯化钠、葡萄糖的物质的量,再根据c=
计算出NaCl和葡萄糖的物质的量浓度.
| m |
| M |
| n |
| V |
解答:
解:4.9g氯化钠的物质的量为:n(NaCl)=
≈0.084mol,
该溶液中氯化钠的物质的量浓度为:c(NaCl)
=0.168mol/L;
25g葡萄糖的物质的量为:n(C6H12O6)=
≈0.139mol,
该溶液中葡萄糖的物质的量浓度为:c(C6H12O6)=
=0.278mol/L,
答:该溶液中NaCl和葡萄糖的物质的量浓度分别为0.168mol/L、0.278mol/L.
| 4.9g |
| 58.5g/mol |
该溶液中氯化钠的物质的量浓度为:c(NaCl)
| 0.084mol |
| 0.5L |
25g葡萄糖的物质的量为:n(C6H12O6)=
| 25g |
| 180g/mol |
该溶液中葡萄糖的物质的量浓度为:c(C6H12O6)=
| 0.139mol |
| 0.5mol |
答:该溶液中NaCl和葡萄糖的物质的量浓度分别为0.168mol/L、0.278mol/L.
点评:本题考查了物质的量浓度计算,题目难度不大,试题侧重基础知识考查,注意掌握物质的量浓度的概念及计算方法,明确物质的量与摩尔质量、物质的量浓度的转化关系为解答关键.

练习册系列答案
相关题目
下列说法正确的是( )
| A、1molO的质量是32g |
| B、HCl相对分子质量36.5g/mol |
| C、SO42-的摩尔质量是96g/mol |
| D、Na的摩尔质量23 |
足量的铜与浓硫酸反应,当反应停止后,加入下列物质后,铜又能继续溶解的是( )
①稀硫酸 ②氧化铁 ③铁 ④硝酸 ⑤硝酸钾.
①稀硫酸 ②氧化铁 ③铁 ④硝酸 ⑤硝酸钾.
| A、②④⑤ | B、①④⑤ |
| C、③④ | D、③④⑤ |
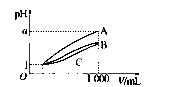 pH=1的三种酸溶液A、B、C各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )
pH=1的三种酸溶液A、B、C各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )| A、溶液的物质的量浓度C>B>A |
| B、酸性A>B>C |
| C、若a=4,则A是强酸,B、C是弱酸 |
| D、若1<a<4,则A、B、C都是弱酸 |
已知氧化性Fe3+>I2.FeI2溶液中通入一定量的Cl2,发生反应的离子方程式为:a Fe2++bI-+c Cl2→d Fe3++e I2+f Cl-下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A、2 4 3 2 2 6 |
| B、0 2 1 0 1 2 |
| C、2 0 1 2 0 2 |
| D、2 10 6 2 5 12 |
下列变化中,不可能通过一步反应实现的是( )
| A、Cu→CuSO4 |
| B、Fe→FeCl3 |
| C、NH3→NO |
| D、SiO2→H2SiO3 |