题目内容
将铜粉放入稀硫酸中,加热无明显现象发生.但加入某盐后,发现铜粉质量逐渐减少,则该盐可能是( )
①ZnSO4 ②Fe2(SO4)3 ③NaCl ④KNO3.
①ZnSO4 ②Fe2(SO4)3 ③NaCl ④KNO3.
| A、①② | B、②③ | C、③④ | D、②④ |
考点:铜金属及其重要化合物的主要性质,硝酸的化学性质,铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:铜粉与稀硫酸不反应,可以与稀硝酸反应,原来溶液中存在氢离子,有硝酸根离子存在时具有强氧化性,此外铜还可以和三价铁反应.
解答:
解:①金属铜和稀硫酸不反应,加入硫酸锌也不反应,故①不选;
②金属铜可以和三价铁离子之间反应生成铜离子和亚铁离子,故②选;
③金属铜和稀盐酸、稀硫酸之间均不反应,所以加入氯化钠,不发生反应,故③不选;
④加入硝酸钾在酸性条件下,有很强的氧化性,能和金属铜之间反应,发生反应的离子方程式应该是:8H++2NO3-+3Cu=3Cu2++4H2O+2NO↑,故④选;
故选D.
②金属铜可以和三价铁离子之间反应生成铜离子和亚铁离子,故②选;
③金属铜和稀盐酸、稀硫酸之间均不反应,所以加入氯化钠,不发生反应,故③不选;
④加入硝酸钾在酸性条件下,有很强的氧化性,能和金属铜之间反应,发生反应的离子方程式应该是:8H++2NO3-+3Cu=3Cu2++4H2O+2NO↑,故④选;
故选D.
点评:铜粉与稀硝酸可以反应,可以直接加入硝酸,也可以先加盐酸或硫酸,再加入硝酸盐,其作用是一样的.

练习册系列答案
相关题目
将ag光亮的铜丝在空气中加热一段时间后,迅速插入足量的下列物质中,取出干燥,如此反复几次,最后取出铜丝用蒸馏水洗涤、干燥、称得其质量为bg.下列所插物质与铜丝的质量关系不正确的是( )
| A、CO a>b |
| B、乙醇溶液 a=b |
| C、NaHSO4 a>b |
| D、石灰水 a<b |
某溶液中可能存在Na+、Mg2+、Al3+、Br-、I-、C
、S
等七种离子中的几种.现取该溶液进行实验,得到如下实验现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
据此可以推断,该溶液中肯定不存在的离子是( )
| O | 2- 3 |
| O | 2- 3 |
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
据此可以推断,该溶液中肯定不存在的离子是( )
A、Al3+、Mg2+、S
| ||||
B、Mg2+、Na+、C
| ||||
C、Al3+、Na+、S
| ||||
D、Al3+、C
|
从节约原料和防止环境污染因素考虑,用铜制取硝酸铜,方法最佳的是( )
A、Cu
| |||||
B、Cu
| |||||
C、Cu
| |||||
D、Cu
|
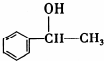 所示.
所示.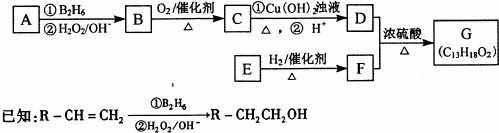
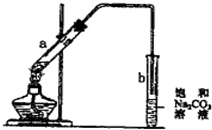 “酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.回答下列问题:
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.回答下列问题: