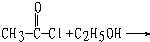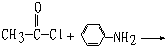题目内容
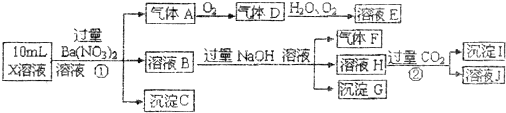
2013年1月全国近二十个省区市遭遇雾霾天气,雾霾天气影响着人们的生活和生命安全.二氧化硫、氮氧化物和可吸入颗粒物这三项是雾霾的主要组成.大气中硫、氮的氧化物还是形成酸雨的主要物质.据测定某地酸雨pH最低达到pH=4,酸雨中还可能含有下列离子:Na+、Ba2+、NH+4、A13+、Cl-、SO32-、SO42-、NO-3等.某研究小组取该地一定量的酸雨,浓缩104倍后将所得澄清试液分成4份,每份各l0mL,进行如下实验
请回答下列问题:
(1)根据实验结果判断该酸雨中肯定不存在的离子是: .不能确定的离子是: _.若要确定是否含有该离子,简单的实验方法是 .
(2)写出下列反应的离子方程式
①试液中滴加淀粉KI溶液时: .
②第三份试液滴加NaOH溶液过程中的AB段: .
(3)经测定结果分析,某地酸雨中含有的部分离子浓度:C(Cl3+)= mol/L c(Al3+)= mol/L
(4)常温下Al(OH)3的Ksp=2.0×10-33,当该地酸雨中的Al3+开始沉淀时的pH至少达到 (忽略加入碱时溶液体积发生的变化).
| 试样 | 所加试剂 | 实验现象及测定数值 |
| 第一份试液 | 滴加适量的淀粉KI溶液 | 溶液呈蓝色 |
| 第二份试液 | 滴加过量的盐酸酸化的BaCl2溶液 | 白色沉淀0.932g |
| 第三份试液 | 滴加0.01mol/LNaOH溶液体积V,与生成沉淀的关系,如右图 | 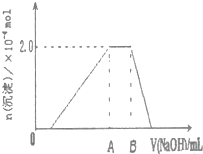 |
| 第四份试液 | 滴加过量的AgNO3 | 白色沉淀1.535g |
(1)根据实验结果判断该酸雨中肯定不存在的离子是:
(2)写出下列反应的离子方程式
①试液中滴加淀粉KI溶液时:
②第三份试液滴加NaOH溶液过程中的AB段:
(3)经测定结果分析,某地酸雨中含有的部分离子浓度:C(Cl3+)=
(4)常温下Al(OH)3的Ksp=2.0×10-33,当该地酸雨中的Al3+开始沉淀时的pH至少达到
考点:常见阴离子的检验,常见阳离子的检验
专题:
分析:滴加适量的淀粉KI溶液,呈蓝色,说明在该酸性溶液中有一种能将碘离子氧化为碘单质的离子存在,而这样的离子只有NO3-,故一定含有NO3-,就一定不会含有SO32-,因为SO32-具有较强的还原性,酸性条件下,与NO3-不能共存;滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出,故一定含有SO42-,一定不含Ba2+,滴加NaOH溶液AB段无沉淀生成,故一定含有NH4+,加入氢氧化钠溶液,有沉淀产生,直至消失,一定含Al3+,白色沉淀0.932g可知硫酸根的物质的量为0.004mol;0.004mol硫酸银的质量为0.004mol×312g/mol=1.248g,滴加过量的AgNO3有白色沉淀1.535g,说明有氯离子,而钠离子的存在与否不能判断.
解答:
解:(1)该酸雨中肯定不存在的离子是SO32-、Ba2+;不能确定的离子是Na+;钠离子的存在可用焰色反应判断,故答案为:SO32-、Ba2+;Na+;焰色反应;
(2)硝酸氧化碘离子的离子方程式为:6I-+2NO3-+8H+=3I2+2NO↑+4H2O;AB段是铵根与氢氧根反应生成氨气:NH4++OH-=NH3↑+H2O,故答案为:6I-+2NO3-+8H+=3I2+2NO↑+4H2O;NH4++OH-=NH3↑+H2O;
(3)白色沉淀0.932g可知硫酸根的物质的量为0.004mol;0.004mol硫酸银的质量为0.004mol×312g/mol=1.248g.
氯化银的质量为1.535g-1.248g=0.287g,物质的量为
=2×10-3mol;n(Cl-)=
=2×10-7mol,c(Cl-)=
=2×10-5mol/L;
根据图知沉淀的最大量为2×10-4mol,n(Cl-)=
=2×10-8mol,c(Al3+)=
=2×10-6mol/L,故答案为:2×10-5;2×10-6;
(4)设溶液的pH为X,氢氧根的浓度为10X-14,Ksp=2.0×10-33=2×10-6mol/L×(10X-14)3,
解得X=5,故答案为:5.
(2)硝酸氧化碘离子的离子方程式为:6I-+2NO3-+8H+=3I2+2NO↑+4H2O;AB段是铵根与氢氧根反应生成氨气:NH4++OH-=NH3↑+H2O,故答案为:6I-+2NO3-+8H+=3I2+2NO↑+4H2O;NH4++OH-=NH3↑+H2O;
(3)白色沉淀0.932g可知硫酸根的物质的量为0.004mol;0.004mol硫酸银的质量为0.004mol×312g/mol=1.248g.
氯化银的质量为1.535g-1.248g=0.287g,物质的量为
| 0.287g |
| 143.5g/mol |
| 2×10-3mol |
| 104 |
| 2×10 -7mol |
| 0.01L |
根据图知沉淀的最大量为2×10-4mol,n(Cl-)=
| 2×10-4mol |
| 104 |
| 2×10-8mol |
| 0.01L |
(4)设溶液的pH为X,氢氧根的浓度为10X-14,Ksp=2.0×10-33=2×10-6mol/L×(10X-14)3,
解得X=5,故答案为:5.
点评:本题考查制备实验方案的设计,涉及离子检验和离子共存方面的知识,为高频考点,把握物质的性质等为解答的关键,侧重分析与实验、计算能力的综合考查,题目难度不大.

练习册系列答案
相关题目
有一无色溶液,可能含有K+、Al3+、Mg2+、NH 4+Cl-SO42- HCO3-、Ba2+中的几种.为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,只产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生.下列推断正确的是( )
| A、肯定没有NH4+、HCO3-、Ba2+ |
| B、可能有K+、Cl-、HCO3- |
| C、肯定有Al3+、Mg2+、SO42-、NH4+ |
| D、若另取部分原溶液加入足量AgNO3溶液有白色沉淀生成,证明原溶液中一定有Cl- |
化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A、太阳能电池板中的硅,在元素周期表中处于金属与非金属的交界位置 |
| B、煤的气化或液化技术,可以降低污染 |
| C、镁粉可用来作信号弹和烟花,氧化镁可制作耐高温材料 |
| D、NaHCO3能与碱反应,因此食品工业用小苏打做焙制糕点的膨松剂 |
 所示.
所示.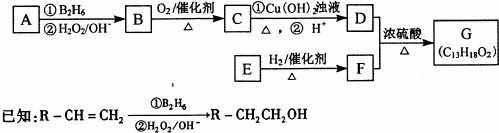
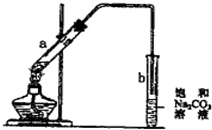 “酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.回答下列问题:
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.回答下列问题: