��Ŀ����
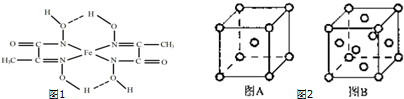
10����A��B��C��D��E���ֶ���������Ԫ�أ�ԭ�Ӱ뾶���μ�С��EԪ��������Ԫ�ز���ͬһ���ڣ�C��D�����ڱ��д�������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮A��Bͬ���ڣ�A2 B�����ӻ������ش���1��A2 B������Ϊ���ƣ�C��E�γɵľ���10���ӵ�4�˷��ӵĽṹʽΪ
 ��
����2������������Ԫ���е�ij����Ԫ�����γɵľ���Ư�����õ����ʵĻ�ѧʽ�ǣ�SO2��H2O2 ��Na2O2������дһ�֣���
��3��B������������ˮ�����Ũ��Һ��ǿ�����ԣ�����ʱ����ͭ�ɱ����������÷�Ӧ�Ļ�ѧ����ʽΪ2H2SO4 ��Ũ��+Cu$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
��4������������Ԫ������������γɵĻ������У���Щ��������ˮ��Ӧ��������������������ԭ��Ӧ����д������һ����Ӧ�Ļ�ѧ����ʽ2Na2 O2+2H2O=4 NaOH+O2�� �� 3NO 2+H2 O=2HNO 3+NO��
���� ��A��B��C��D��E���ֶ���������Ԫ�أ�ԭ�Ӱ뾶���μ�С��C��D�����ڱ��д�������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壬��CΪNԪ�ء�DΪOԪ�أ�EԪ��������Ԫ�ز���ͬһ���ڣ���E��ԭ�Ӱ뾶С��������EΪHԪ�أ�A��Bͬ���ڣ�A2 B�����ӻ����AΪ+1�ۣ�BΪ-2�ۣ���AΪNa��BΪSԪ�أ�
��� �⣺��A��B��C��D��E���ֶ���������Ԫ�أ�ԭ�Ӱ뾶���μ�С��C��D�����ڱ��д�������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壬��CΪNԪ�ء�DΪOԪ�أ�EԪ��������Ԫ�ز���ͬһ���ڣ���E��ԭ�Ӱ뾶С��������EΪHԪ�أ�A��Bͬ���ڣ�A2 B�����ӻ����AΪ+1�ۣ�BΪ-2�ۣ���AΪNa��BΪSԪ�أ�
��1��A2 BΪNa2S������Ϊ���ƣ�C��E�γɵľ���10���ӵ�4�˷���ΪNH3���ṹʽΪ ��
��
�ʴ�Ϊ�����ƣ� ��
��
��2������������Ԫ���е�ij����Ԫ�����γɵľ���Ư�����õ����ʵĻ�ѧʽ�ǣ�SO2��H2O2 ��Na2O2��
�ʴ�Ϊ��SO2��H2O2 ��Na2O2��
��3��Cu��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��2H2SO4 ��Ũ��+Cu$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
�ʴ�Ϊ��2H2SO4 ��Ũ��+Cu$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
��4������������Ԫ������������γɵĻ������У���Щ��������ˮ��Ӧ��������������������ԭ��Ӧ������һ����Ӧ�Ļ�ѧ���̣�2Na2 O2+2H2O=4 NaOH+O2�� �� 3NO 2+H2 O=2HNO 3+NO��
�ʴ�Ϊ��2Na2 O2+2H2O=4 NaOH+O2�� �� 3NO 2+H2 O=2HNO 3+NO��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ�����Ҫѧ����������Ԫ�ػ�����֪ʶ���Ѷ��еȣ�

 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д�| A�� | ������������Һ�еμ�����������Һ��Ba2++2OH-+2H++SO42-=BaS04��+2H2O | |
| B�� | ���Խ�����KMnO4���� H2O2��2MnO4-+5H2O2+6H+=2Mn2++5O2��+8H2O | |
| C�� | NaClO��Һ��ͨ�����SO2��ClO-+SO2+H2O=HClO+HS03- | |
| D�� | ��������Һ�еμ�����Ba��OH��22Al3++3SO42-+3Ba2++6OH-=2Al��OH��3��+3BaSO4�� |
 ���л���X�ļ���ʽΪ
���л���X�ļ���ʽΪ 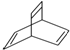 ������˵����ȷ���ǣ�������
������˵����ȷ���ǣ�������| A�� | X�Ļ�ѧʽΪC8H10 | |
| B�� | �л���Y  ��X��Ϊͬϵ�� ��X��Ϊͬϵ�� | |
| C�� | X�����ӳɷ�Ӧ��ʹ���Ը��������Һ��ɫ | |
| D�� | X��������H2��һ�������·�Ӧ�����ɻ�״��Z��Z��һ�ȴ�����2�� |
| A�� | $\frac{��N-M��}{45}$ | B�� | $\frac{��M-N��}{45}$ | C�� | $\frac{��M-N��}{90}$ | D�� | $\frac{��N-M��}{90}$ |
| A�� | Na+��Al3+��SO42-��HCO3- | B�� | Cu2+��Mg2+��SO42-��NO3- | ||
| C�� | Na+��K+��ClO-��SO42- | D�� | Fe3+��K+��SO42-��I- |
| A�� | ������ӵĵ���ʽ�� | B�� | S2-�Ľṹʾ��ͼ�� | ||
| C�� | HClO�Ľṹʽ��H-O-Cl | D�� | NH4Cl�ĵ���ʽ��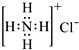 |
| A�� | �ڱ�״���£�22.4L C5H10������̼ԭ����ĿΪ5NA | |
| B�� | ���³�ѹ�£�7.8g�������ƺ��е�������Ϊ0.3NA | |
| C�� | 18gˮ�����ĵ�����ĿΪ10NA | |
| D�� | 3.2g O2��O3�������������ԭ��һ����0.2NA |
| A�� | ���Ϸ�Ӧ | B�� | �û���Ӧ | C�� | ���ֽⷴӦ | D�� | ������ԭ��Ӧ |