题目内容
10.有100mL 3mol•L-1的NaOH溶液和100mL 1mol/L的AlCl3溶液,按如下两种方法进行实验:①将NaOH溶液分多次加入到AlCl3溶液中(边加边搅拌);
②将AlCl3溶液分多次加入到NaOH溶液中(边加边搅拌).
比较两次实验的结果,其中正确的是( )
| A. | 现象相同,沉淀量相等 | B. | 现象不同,沉淀量不等 | ||
| C. | 现象相同,沉淀量不等 | D. | 现象不同,沉淀量相等 |
分析 NaOH溶液分多次加到AlCl3溶液中,发生Al3++3OH-═Al(OH)3↓,将AlCl3溶液分多次加到NaOH溶液中,分别发生Al3++4OH-=AlO2-+2H2O,Al3++3AlO2-+6H2O=4Al(OH)3↓,以此进行判断.
解答 解:100mL 3mol•L-1NaOH溶液中n(NaOH)=0.3mol,100mL 1mol•L-1的AlCl3溶液中n(AlCl3)=0.1mol,则
①将NaOH溶液分多次加到AlCl3溶液中,发生:Al3++3OH-═Al(OH)3↓,现象为观察到白色沉淀;
②将AlCl3溶液分多次加到NaOH溶液中,分别发生:Al3++4OH-=AlO2-+2H2O,Al3++3AlO2-+6H2O=4Al(OH)3↓,先没有沉淀后出现沉淀,
所以二者现象不同,由于AlCl3最后全部转化为Al(OH)3,沉淀质量相等.
故选D.
点评 本题考查钠的化合物的性质,为高频考点,侧重学生的分析能力的考查,题目难度不大,学习中注意相关基础知识的积累,特别是铝三角知识,为中学元素化合物中的重要内容.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
1.已知NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O+CO2↑,则150℃时NH4HCO3分解产生的混合气体A的密度是相同条件下H2密度的( )倍.
| A. | 26.3 | B. | 13.2 | C. | 19.8 | D. | 无法计算 |
18.NA代表阿伏加德罗常数,下列说法中,正确的是( )
| A. | 2.7g金属铝变成铝离子时失去的电子数目为0.1NA (提示:M(Al)=27g/mol) | |
| B. | 17g氨气所含的电子数目为10NA (提示:M(NH3)=17g/mol) | |
| C. | 2g氢气所含原子数目为NA (提示:M(H2)=2g/mol) | |
| D. | 常温常压下,11.2L氮气所含的原子数目为NA |
5.火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2=Cu2S+2FeS+SO2下列说法正确的是( )
| A. | SO2既是氧化产物又是还原产物 | |
| B. | CuFeS2仅作还原剂,硫元素被氧化 | |
| C. | 每生成1mol Cu2S,有4 mol硫被氧化 | |
| D. | 每转移1.2 mol电子,有0.3 mol硫被氧化 |
15.下列分离提纯方法不正确的是( )
| A. | 分离乙酸和乙酸乙酯,常用蒸馏法 | |
| B. | 提纯含有碘的氯化铵,常用升华法 | |
| C. | 除去碳酸钠中的少量碳酸氢钠,常用加热法 | |
| D. | 除去CO2中的SO2,通过盛有溴水的洗气瓶 |
1.实验室里临时要用NaOH溶液和CO2来制取纯Na2CO3溶液.已知CO2气体通入NaOH溶液过程中极易生成过量NaHCO3,且无明显现象.实验室有下列试剂:①未知浓度的NaOH溶液 ②37%的盐酸 ③37%的硫酸 ④14%盐酸 ⑤大理石⑥K2CO3固体 ⑦Cu2(OH)2CO3
实验室有下列仪器:铁架台、启普发生器、量筒、烧杯、橡皮管、玻璃导管、分液漏斗.
已知下表中各物质在常温时的溶解度(g/100g水)
(1)本实验应选用的仪器除启普发生器、橡皮管、玻璃导管外,还需要烧杯、量筒.
(2)为保证制得的Na2CO3溶液尽量纯,应选用的药品(填编号)除①外,还需要④⑤.
(3)简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装可省略)①量取一定量的NaOH溶液,分成两等份②制取CO2,向其中一份NaOH溶液中通入过量的CO2气体③将两溶液混合均匀.
(4)根据给出的溶解度表,求出当NaOH溶液中溶质的质量分数大于多少时,在配制过程中会有晶体析出(写出计算步骤和必要的文字说明)
实验室有下列仪器:铁架台、启普发生器、量筒、烧杯、橡皮管、玻璃导管、分液漏斗.
已知下表中各物质在常温时的溶解度(g/100g水)
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
(2)为保证制得的Na2CO3溶液尽量纯,应选用的药品(填编号)除①外,还需要④⑤.
(3)简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装可省略)①量取一定量的NaOH溶液,分成两等份②制取CO2,向其中一份NaOH溶液中通入过量的CO2气体③将两溶液混合均匀.
(4)根据给出的溶解度表,求出当NaOH溶液中溶质的质量分数大于多少时,在配制过程中会有晶体析出(写出计算步骤和必要的文字说明)
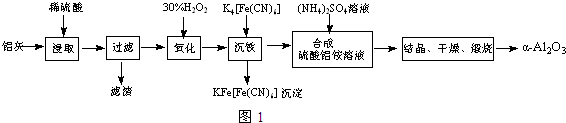
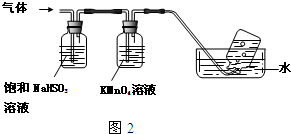 (2)加30%的H2O2溶液的目的是氧化Fe2+为Fe3+,有利于在沉铁过程中除去.
(2)加30%的H2O2溶液的目的是氧化Fe2+为Fe3+,有利于在沉铁过程中除去.
