题目内容
1.已知NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O+CO2↑,则150℃时NH4HCO3分解产生的混合气体A的密度是相同条件下H2密度的( )倍.| A. | 26.3 | B. | 13.2 | C. | 19.8 | D. | 无法计算 |
分析 先根据NH4HCO3分解求出混合气体的平均摩尔质量,然后利用密度之比等于摩尔质量之比计算,以此解答.
解答 解:设NH4HCO3为1mol,由方程式NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑可知,生成NH3、H2O、CO2气体各为1mol,则混合气平均摩尔质量为$\frac{(17+18+44)g}{3mol}$=26.33g/mol,因氢气密度之比等于摩尔质量之比,所以混合气的密度是相同条件下的氢气密度的$\frac{26.33}{2}$=13.2,
故选B.
点评 本题结合铵盐的化学性质,为高频考点,考查了阿伏伽德罗定律推论应用等,有利于培养学生的分析能力和计算能力,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
11.对于可逆反应3H2+N2?2NH3,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
| A. | 使用高效催化剂 | B. | 充入更多N2 | C. | 降低温度 | D. | 增大压强 |
12.工业制备氯化铜时,将浓盐酸加热至80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤.请回答以下问题:
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
(1)将浓盐酸溶解粗CuO粉末后,溶液中的金属阳离子含有Cu2+、Fe2+、Fe3+、H+,第一步除去该溶液中的Fe2+,能否直接调整溶液pH=9.6,将Fe2+沉淀除去?不能,(填“能”或“不能”)理由是因Fe2+沉淀的pH最大,Fe2+沉淀完全时,Cu2+、Fe3+也会沉淀完全
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的PH将Fe3+沉淀除去:你认为用NaClO作氧化剂是否妥当?否(填“是”或“否”),现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有BD(有几个选几个,填代号,下同).
A.浓HNO3 B.Cl2 C.KMnO4 D.H2O2
(3)①加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的AD.
A.CuO B.NH3•H2O C.NaOH D.Cu(OH)2
②加上述物质调节溶液的PH为3.2~4.7,原因是铁离子沉淀完全时的PH值为3.2,铜离子开始沉淀时的PH值为4.7,除杂时要使铁离子沉淀完全,不能使铜离子产生沉淀
(4)最后能不能直接将溶液蒸发得到CuCl2•2H2O?不能(填“能”或者“不能”).若不能,应该如何操作才能得到CuCl2•2H2O应在氯化氢气氛中浓缩后冷却结晶(若填“能”,此空不用回答)
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9 | 6.7 |
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的PH将Fe3+沉淀除去:你认为用NaClO作氧化剂是否妥当?否(填“是”或“否”),现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有BD(有几个选几个,填代号,下同).
A.浓HNO3 B.Cl2 C.KMnO4 D.H2O2
(3)①加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的AD.
A.CuO B.NH3•H2O C.NaOH D.Cu(OH)2
②加上述物质调节溶液的PH为3.2~4.7,原因是铁离子沉淀完全时的PH值为3.2,铜离子开始沉淀时的PH值为4.7,除杂时要使铁离子沉淀完全,不能使铜离子产生沉淀
(4)最后能不能直接将溶液蒸发得到CuCl2•2H2O?不能(填“能”或者“不能”).若不能,应该如何操作才能得到CuCl2•2H2O应在氯化氢气氛中浓缩后冷却结晶(若填“能”,此空不用回答)
9.某小组探究Na2CO3和NaHCO3的性质,实验步骤及记录如下:
Ⅰ.分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1;
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度T3.
得到表1的数据:
表1
回答下列问题:
(1)Na2CO3溶于水显碱性,其原因是CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-(用离子方程式表示).
(2)根据试题后的附表判断:
步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解Na2CO3、NaHCO3固体都是全部溶解.
(3)分析表1的数据得出:Na2CO3固体溶于水放热,NaHCO3固体溶于水吸热
(填“放热”或“吸热”).
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应.
乙同学认为应该增加一个实验,并补做如下实验:向 盛 有10 mL水(20℃)的烧杯中加入10mL密度约为1.1g/mL20%的盐酸,搅拌,测量温度为22.2℃.
(5)结合上述探究,下列说法正确的是AC.
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1 g混合物,加热至质量不变时,称其质量为m2 g,则原混合物中NaHCO3的质量分数为$\frac{84(m{\;}_{1}-m{\;}_{2})}{31m{\;}_{1}}$×100%(用代数式表示).
附表:溶解度表
Ⅰ.分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1;
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度T3.
得到表1的数据:
表1
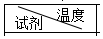 | T1/℃ | T2/℃ | T3/℃ |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
(1)Na2CO3溶于水显碱性,其原因是CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-(用离子方程式表示).
(2)根据试题后的附表判断:
步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解Na2CO3、NaHCO3固体都是全部溶解.
(3)分析表1的数据得出:Na2CO3固体溶于水放热,NaHCO3固体溶于水吸热
(填“放热”或“吸热”).
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应.
乙同学认为应该增加一个实验,并补做如下实验:向 盛 有10 mL水(20℃)的烧杯中加入10mL密度约为1.1g/mL20%的盐酸,搅拌,测量温度为22.2℃.
(5)结合上述探究,下列说法正确的是AC.
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1 g混合物,加热至质量不变时,称其质量为m2 g,则原混合物中NaHCO3的质量分数为$\frac{84(m{\;}_{1}-m{\;}_{2})}{31m{\;}_{1}}$×100%(用代数式表示).
附表:溶解度表
 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
10.有100mL 3mol•L-1的NaOH溶液和100mL 1mol/L的AlCl3溶液,按如下两种方法进行实验:
①将NaOH溶液分多次加入到AlCl3溶液中(边加边搅拌);
②将AlCl3溶液分多次加入到NaOH溶液中(边加边搅拌).
比较两次实验的结果,其中正确的是( )
①将NaOH溶液分多次加入到AlCl3溶液中(边加边搅拌);
②将AlCl3溶液分多次加入到NaOH溶液中(边加边搅拌).
比较两次实验的结果,其中正确的是( )
| A. | 现象相同,沉淀量相等 | B. | 现象不同,沉淀量不等 | ||
| C. | 现象相同,沉淀量不等 | D. | 现象不同,沉淀量相等 |

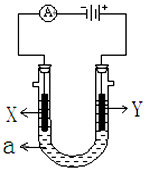 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
 .
.