题目内容
下列说法中正确的是( )
| A、双原子分子中化学键键能越大,分子越牢固 |
| B、双原子分子中化学键键长越长,分子越牢固 |
| C、双原子分子中化学键键角越大,分子越牢固 |
| D、同一分子中,σ健与π健的分子轨道重叠程度一样多,只是重叠的方向不同 |
考点:键能、键长、键角及其应用
专题:化学键与晶体结构
分析:分子的稳定性与共价键的键长、键能有关,σ键比π键稳定,σ键的重叠程度比π键的分子轨道重叠程度大,据此分析.
解答:
解:A、双原子分子中化学键键能越短,键能越大,分子越牢固,故A正确;
B、双原子分子中化学键键能越长,键能越小,分子越不牢固,故B错误;
C、不能根据键角的大小来判断分子的稳定性,故C错误;
D、原子轨道通过头碰头的重叠形成σ键,通过肩并肩的重叠形成π键,σ键的重叠程度比π键的重叠程度大,故D错误;
故选A.
B、双原子分子中化学键键能越长,键能越小,分子越不牢固,故B错误;
C、不能根据键角的大小来判断分子的稳定性,故C错误;
D、原子轨道通过头碰头的重叠形成σ键,通过肩并肩的重叠形成π键,σ键的重叠程度比π键的重叠程度大,故D错误;
故选A.
点评:本题考查了分子的稳定性的判断、共价键的类型,题目难度不大,注意把握影响分子稳定性的因素.

练习册系列答案
相关题目
已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是( )
| A、16 g |
| B、32 g |
| C、64 g/mol |
| D、32 g/mol |
在水溶液中能大量共存的一组离子或离子分子组是( )
| A、I2、SO32-、Cl-、Na+ |
| B、K+、Cu2+、OH-、NO3- |
| C、NH4+、Na+、Br-、SO42- |
| D、Ag+、NH3*H2O、NO3-、Na+ |
下列化学用语表达正确的是( )
A、丙烷分子的球棍模型: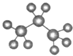 |
B、Na2S的电子式: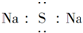 |
| C、乙烯的结构简式:CH2CH2 |
| D、氯仿的化学式:CCl4 |
A、B两元素可形成AB型离子化合物,且阴、阳离子具有相同的电子数.A、B的单质均能与水发生剧烈反应,反应中A单质做还原剂,B单质做氧化剂,则下列表述正确的是( )
| A、B元素原子的电子排布式为1S22S22P63S23P5 |
B、化合物AB的电子式为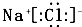 |
C、化合物AB的电子式为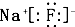 |
| D、A与水反应的离子方程式为Na+H2O═OH-+Na++H2 |
下列有关化学概念或原理的论述中,正确的是( )
| A、任何一个氧化还原反应都可以设计为电池,输出电能 |
| B、铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
| C、电解饱和食盐水的过程中,水的电离平衡正向移动 |
| D、任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大 |
同温同压下,同体积的CO和CO2,下列说法不正确的是( )
| A、分子数之比等于2:3 |
| B、原子数之比等于2:3 |
| C、气体物质的量之比等于1:1 |
| D、质量之比等于7:11 |