题目内容
16.将镁条在空气中燃烧的全部产物(由于空气中CO2含量少,镁条与CO2反应忽略不计)溶解在50mL浓度为1.8mol/L的盐酸中,以20mL0.9mol/L的NaOH溶液中和多余的酸,然后向溶液中加入过量的NaOH并加热,把生成的氨全部蒸发出来,用足量盐酸吸收,经测定氨的质量为0.102g,试计算原镁条的质量.分析 加入碱前,体系是含Mg2+、Na+、NH4+、Cl-的电解质溶液,依电荷守恒得:2n(Mg2+)+n(Na+)+n(NH4+)=n(Cl-).
根据氮元素守恒有n(NH4+)=n(NH3),根据氯原子守恒有n(Cl-)=n(HCl),根据钠原子守恒有n(Na+)=n(NaOH),计算出n(NH4+)、n(Cl-)、n(Na+),代入电荷守恒等式计算出n(Mg2+),根据镁元素守恒可知n(Mg)=n(Mg2+),再利用m=nM计算镁条质量.
解答 解:加入热碱前,体系是含Mg2+、Na+、NH4+、Cl-的电解质溶液,溶液中:
n(Cl-)=n(HCl)=1.8 mol•L-1×0.05L=0.09mol,
n(Na+)=n(NaOH)=0.9 mol•L-1×0.02L=0.018mol,
n(NH4+)=n(NH3)=$\frac{0.102g}{17g/mol}$=0.006 mol,
依电荷守恒得:2n(Mg2+)+n(Na+)+n(NH4+)=n(Cl-),所以2n(Mg2+)+0.018mol+0.006mol=0.09,
解得n(Mg2+)=0.033mol,所以n(Mg)=n(Mg2+)=0.033mol,故镁条的质量 m(Mg)=0.033mol×24g/mol=0.792g,
答:原镁条的质量为0.792g.
点评 本题考查混合物、根据方程式的计算等,难度较大,清楚反应过程,利用电荷守恒进行解答是关键,注意守恒思想在计算中的运用.

练习册系列答案
相关题目
5.实验室不需要用棕色试剂瓶保存的试剂是( )
| A. | 浓硝酸 | B. | 硝酸银 | C. | 氯水 | D. | 氨水 |
4.甲醇是一种很好的燃料,工业上用CH4和H2O(g)为原料,通过反应Ⅰ和Ⅱ来制备甲醇.请回答下列问题:
(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L)中,在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)(Ⅰ)
CH4的转化率与温度、压强的关系如图1所示.
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为0.003mol•L-1•min-1.
②图中的p1<p2(填“<”、“>”或“=”),100℃时的平衡常数为2.25×10-4.
③该反应的△H>0,△S>0(填“<”、“>”或“=”).
(2)在压强为0.1MPa条件下,a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:
CO(g)+2H2(g)?CH3OH△H<0 (Ⅱ)
①若容器的容积不变,下列措施可增大甲醇产率的是ABD(填序号).
A.降低温度
B.将CH3OH(g)从体系中分离出来
C.恒容下充入He,使体系的总压强增大
D.再充入a mol CO和3a mol H2
②为了寻找合成甲醇的适宜温度和压强,某同学设计了三组实验,部分实验条件已经填在了下面的实验设计表中.
a.表中剩余的实验数据:n=180,m=$\frac{2}{3}$.
b.根据反应Ⅱ的特点,如图是在压强分别为0.2MPa和5MPa下CO的转化率随温度变化的曲线,请指明图2中的压强px=0.2MPa.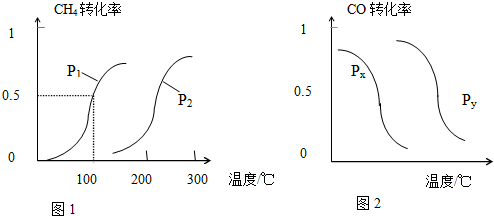
(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L)中,在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)(Ⅰ)
CH4的转化率与温度、压强的关系如图1所示.
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为0.003mol•L-1•min-1.
②图中的p1<p2(填“<”、“>”或“=”),100℃时的平衡常数为2.25×10-4.
③该反应的△H>0,△S>0(填“<”、“>”或“=”).
(2)在压强为0.1MPa条件下,a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:
CO(g)+2H2(g)?CH3OH△H<0 (Ⅱ)
①若容器的容积不变,下列措施可增大甲醇产率的是ABD(填序号).
A.降低温度
B.将CH3OH(g)从体系中分离出来
C.恒容下充入He,使体系的总压强增大
D.再充入a mol CO和3a mol H2
②为了寻找合成甲醇的适宜温度和压强,某同学设计了三组实验,部分实验条件已经填在了下面的实验设计表中.
| 实验编号 | T(℃) | n(CO)/n(H2) | P(MPa) |
| 1 | 180 | $\frac{2}{3}$ | 0.1 |
| 2 | n | $\frac{2}{3}$ | 5 |
| 3 | 350 | m | 5 |
b.根据反应Ⅱ的特点,如图是在压强分别为0.2MPa和5MPa下CO的转化率随温度变化的曲线,请指明图2中的压强px=0.2MPa.

11.已知糖类、油脂和蛋白质提供的能量分别为17.2kJ•g-1、39.3kJ•g-1和18kJ•g-1,下面是花生米和小麦中几种营养素的含量表,
试计算:
(1)比较500g小麦和500g花生米的能量大小.(假设能量能被完全释放)
(2)我们平时所吃的植物油之一就是花生油.将花生米加工后用机器压榨,约有85%的油脂可成为商品花生油.某食品厂购买了100吨花生米,他们可生产多少吨商品花生油?
| 糖类 | 油脂 | 蛋白质 | 其他 | |
| 花生米 | 24% | 39% | 26% | 11% |
| 小麦 | 76% | 2% | 11% | 11% |
(1)比较500g小麦和500g花生米的能量大小.(假设能量能被完全释放)
(2)我们平时所吃的植物油之一就是花生油.将花生米加工后用机器压榨,约有85%的油脂可成为商品花生油.某食品厂购买了100吨花生米,他们可生产多少吨商品花生油?
5.用NA表示阿伏伽德罗常数的数值,下列叙述正确的是( )
| A. | 在同温同压下,相同体积的任何气体单质所含的分子数目一定相同 | |
| B. | 1L 0.5mol/L FeCl3溶液完全转化可得0.5NA个Fe(OH)3胶粒 | |
| C. | 标准状况下,22.4L苯含有的分子数为1NA | |
| D. | 在常温常压下,11.2 L氮气所含的原子数目为NA |