题目内容
1.分子式为CH4、C2H4、C2H2、C6H6、C5H10的烃.物质的量相同时,耗氧量最多的是C6H6、C5H10,生成CO2最多的是C6H6.分析 设分子式为CH4、C2H4、C2H2、C6H6、C5H10的烃的物质的量均为1mol,则
CH4耗氧量为2mol,生成CO21mol,生成水2mol,
C2H4耗氧量为3mol,生成CO22mol,生成水2mol,
C2H2耗氧量为2.5mol,生成CO22mol,生成水1mol,
C6H6耗氧量为7.5mol,生成CO26mol,生成水3mol,
C5H10耗氧量为7.5mol,生成CO25mol,生成水5mol;由此分析解答.
解答 解:设分子式为CH4、C2H4、C2H2、C6H6、C5H10的烃的物质的量均为1mol,则
CH4耗氧量为2mol,生成CO21mol,生成水2mol,
C2H4耗氧量为3mol,生成CO22mol,生成水2mol,
C2H2耗氧量为2.5mol,生成CO22mol,生成水1mol,
C6H6耗氧量为7.5mol,生成CO26mol,生成水3mol,
C5H10耗氧量为7.5mol,生成CO25mol,生成水5mol;
物质的量相同时,耗氧量最多的是C6H6、C5H10,生成CO2最多的是C6H6,故答案为:C6H6、C5H10;C6H6.
点评 本题考查了烃类物质的有关计算,难度中等,侧重于分析能力和计算能力的考查,注意同质量和同物质的量的区别.

练习册系列答案
相关题目
11.羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害.在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)?COS(g)+H2(g),K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )
| A. | 升高温度,H2S浓度增加,表明该反应的△H>0 | |
| B. | 随着反应的进行,混合气体的密度逐渐减小 | |
| C. | 反应前H2S物质的量为7mol | |
| D. | CO的平衡转化率为80% |
6.下列物质,是强电解质的是( )
| A. | 硫酸钡 | B. | 石墨 | C. | 浓盐酸 | D. | HF |
11.下列有关实验装置进行的相应实验,能达到实验目的是( )
| A. | 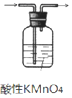 用图 1所示装置除去乙烯中少量 SO2 气体 | |
| B. |  用图 装置量取 20.00 mL 0.10 mol•L-1硫酸 | |
| C. | 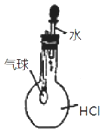 用图 装置能验证 HCl 气体在水中的溶解性 | |
| D. | 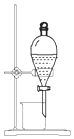 用图 装置从碘的 CCl4溶液中分离出碘 |
 如图所示图象中.纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,按试题将相应图的字母填入下列空格.
如图所示图象中.纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,按试题将相应图的字母填入下列空格.