题目内容
16.现有两种气态烃的混合气体,通过不同实验分别测出下列数据①1mol该混合烃,在空气中燃烧得到1.5molCO2;
②125℃时,1L某气态烃在9L氧气中充分燃烧反应后的混合气体体积仍为10L(相同条件下);
③0.3moL混和烃完全燃烧生成10.8gH2O;
④相同条件下,该混合烃的密度是氢气的 10倍;
⑤实验测出混合气体中碳原子和氢原子的比值为1:3
⑥60g混合烃完全燃烧生成108gH2O.
上述数据可以直接说明混合烃中一定存在甲烷的是( )
| A. | ①②③④⑤⑥ | B. | ①②③⑥ | C. | ③④⑤⑥ | D. | ①④⑤⑥ |
分析 ①计算平均碳原子数目判断;
②反应燃烧前后气体的体积不变(水为气体),则平均分子式中H原子数目为4,可以为乙烯、丙炔等;
③计算平均H原子数目判断;
④由相对氢气密度,可知混合烃的平均相对分子质量为20;
⑤混合气体C、H原子数目之比1:3,而小于1:3的只有甲烷;
⑥计算水的物质的量,可得混合气体中H原子物质的量,结合混合气体总质量计算C原子物质的量,再结合C、H原子数目之比判断.
解答 解:①混合气体平均碳原子数目为$\frac{1.5mol×1}{1mol}$=1.5,所有烃中只有甲烷的碳原子数目小于1.5,则一定含有甲烷,故选;
②设平均分子式为CxHy,则:CxHy+(x+$\frac{y}{4}$)$\frac{\underline{\;点燃\;}}{\;}$xCO2+$\frac{y}{2}$H2O(g),反应燃烧前后气体的体积不变,则1+(x+$\frac{y}{4}$)=x+$\frac{y}{2}$,故y=4,甲烷、乙烯、丙炔等分子中都含有4个H原子,不一定含有甲烷,故不选;
③水的物质的量为$\frac{10.8g}{18g/mol}$=0.6mol,则分平均H原子数目为$\frac{0.6mol×2}{0.3mol}$=4,甲烷、乙烯、丙炔等分子中都含有4个H原子,不一定含有甲烷,故不选;
④由相对氢气密度,可知混合烃的平均相对分子质量为10×2=20,烃中相对分子质量小于20的只有甲烷,则一定含有甲烷,故选
⑤混合气体C、H原子数目之比1:3,而小于1:3的只有甲烷,故选;
⑥水的物质的量为$\frac{108g}{18g/mol}$=6mol,氢原子物质的量为12mol,则C原子物质的量为$\frac{60g-12mol×1g/mol}{12g/mol}$4mol,混合气体C、H原子数目之比1:3,而小于1:3的只有甲烷,故选.
故选:D.
点评 本题考查有机物分子式确定、混合物计算,注意利用平均值解答,常用平均值有:平均碳法、平均氢法、平均分子式、平均相对分子质量、平均碳氢法的等.

| A. | 沸点:正戊烷>2-甲基丁烷>乙烷 | B. | 同分异构体种类:戊烯<戊烷 | ||
| C. | 密度:苯<水<硝基苯 | D. | 含碳量:乙烯>乙烷 |
| A. | $\frac{1}{49}$ | B. | 49 | C. | $\frac{1}{7}$ | D. | 7 |
| A. | 在电流的作用下,氖原子与构成灯管的物质发生反应 | |
| B. | 电子由激发态向基态跃迁时以光的形式释放能量 | |
| C. | 氖原子获得电子后转变成发出红光的物质 | |
| D. | 电子由基态向激发态跃迁时吸收除红光以外的光线 |
| A. | X、Y、Z的浓度不再发生变化 | B. | 消耗Z的速率是生成X的速率的2倍 | ||
| C. | 气体总质量保持不变 | D. | X、Y、Z的分子数之比为1:3:2 |
| D | ||
| A | B | C |
| E |
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是(写酸的化学式)H2SO4
(3)上述五种元素的氢化物稳定性最强的是(写氢化物的化学式)H2O,用电子式表示该物质的形成过程
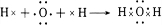 .
. | A. | 同一主族元素的原子序数的差不可能为10 | |
| B. | 同周期第ⅡA族与第ⅢA族元素的原子序数差值一定是1 | |
| C. | 催化剂一般在金属与非金属的分界线处寻找 | |
| D. | 过渡元素全部是金属元素 |
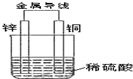
| A. | 铜片上没有气泡产生 | B. | 铜片质量逐渐减少 | ||
| C. | 电流从锌片经导线流向铜 | D. | 氢离子在铜片表面被还原 |

已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO2-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下.
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8(>8溶解) | 9(>9溶解) |
(2)如果把“调pH=8”和“调pH>11”中间的“过滤”步骤省略,引起的后果是pH>11时Al(OH)3会溶解,引入杂质离子AlO2-,使产品不纯.
(3)流程图中“□”内的操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)工业废水中的Na2CrO4遇酸时可转化为Na2Cr2O7,含Cr2O72-的废水毒性较大,为了使废水的排放达标,进行如下处理:

①绿矾化学式为FeSO4•7H20,反应(Ⅰ)的离子方程式为Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O.
②若处理后的废水中c(Cr3+)=3.0×10-6mol•L-1,则废水中c(Fe3+)=2×10-13mol•L-1.
(Ksp[Fe(OH)3])=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)
(5)某工厂为了测定重铬酸钠样品的纯度,称取重铬酸钠试样2.500g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol•L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,再加入淀粉溶液作指示剂,用0.1200mol•L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-).
①判断达到滴定终点的依据是当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色;
②若实验中共用去Na2S2O3标准溶液40.00ml,则该工厂的重铬酸钠样品的纯度为(设整个过程中其它杂质不参与反应)83.84%.