题目内容
现有甲、乙两瓶无色溶液,已知它们可能是NaOH溶液和AlCL3溶液.现做如下实验:
①440mL甲溶液与120mL乙溶液反应,产生1.56沉淀
②120mL甲溶液与440mL乙溶液反应,产生1.56沉淀
③120mL甲溶液与400mL乙溶液反应,产生3.12沉淀
通过必要的计算和推理判定:
甲溶液是 ,其浓度为 mol/L.乙溶液是 其浓度为 mol/L.
①440mL甲溶液与120mL乙溶液反应,产生1.56沉淀
②120mL甲溶液与440mL乙溶液反应,产生1.56沉淀
③120mL甲溶液与400mL乙溶液反应,产生3.12沉淀
通过必要的计算和推理判定:
甲溶液是
考点:镁、铝的重要化合物,化学方程式的有关计算
专题:几种重要的金属及其化合物
分析:由(2)和(3)可知,一定量的甲与乙反应时,乙的量越多,生成的沉淀越少,则乙为NaOH溶液,即甲为AlCl3溶液;
根据(1)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl,碱不足来计算NaOH溶液的物质的量浓度;
根据(2)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,假设出最大沉淀量,并利用生成的沉淀的量来计算AlCl3溶液的浓度.
根据(1)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl,碱不足来计算NaOH溶液的物质的量浓度;
根据(2)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,假设出最大沉淀量,并利用生成的沉淀的量来计算AlCl3溶液的浓度.
解答:
解:由(2)和(3)可知,一定量的甲与乙反应时,乙的量越多,生成的沉淀越少,则乙为NaOH溶液,即甲为AlCl3溶液,
在(1)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl,1.56g沉淀的物质的量为
=0.02mol,碱不足,完全反应,
则NaOH的物质的量为0.02mol×3=0.06mol,故NaOH溶液的物质的量浓度为
=0.5mol/L,
在(2)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,假设出沉淀最大量xmol,开始沉淀过程消耗氢氧根离子3xmol,
沉淀溶解过程氢氧化铝与氢氧化钠1:1反应,最后生成0.02mol氢氧化铝,所以消耗氢氧化钠(x-0.02)mol,
则一共消耗氢氧化钠为3x+(x-0.02)=0.44L×0.5mol/L=0.22mol,解得x=0.06mol,即最多有氢氧化铝0.06mol,所以原溶液含铝离子0.06mol,
氯化铝浓度为
=0.5mol/L,
故答案为:AlCl3;0.5;NaOH;0.5.
在(1)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl,1.56g沉淀的物质的量为
| 1.56g |
| 78g/mol |
则NaOH的物质的量为0.02mol×3=0.06mol,故NaOH溶液的物质的量浓度为
| 0.06mol |
| 0.12L |
在(2)中发生AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O,假设出沉淀最大量xmol,开始沉淀过程消耗氢氧根离子3xmol,
沉淀溶解过程氢氧化铝与氢氧化钠1:1反应,最后生成0.02mol氢氧化铝,所以消耗氢氧化钠(x-0.02)mol,
则一共消耗氢氧化钠为3x+(x-0.02)=0.44L×0.5mol/L=0.22mol,解得x=0.06mol,即最多有氢氧化铝0.06mol,所以原溶液含铝离子0.06mol,
氯化铝浓度为
| 0.06mol |
| 0.12L |
故答案为:AlCl3;0.5;NaOH;0.5.
点评:本题考查氯化铝与碱的反应,明确氢氧化铝的两性及了利用信息判断过量碱能溶解氢氧化铝、实验中发生的化学反应是解答的关键,难度较大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关物质性质、应用的说法中不正确的是( )
| A、Al2O3既能溶于NaOH溶液又能溶于HCl,说明Al2O3是两性氧化物 |
| B、浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性 |
| C、SO2气体具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 |
| D、石英的主要成分是SiO2 |
短周期主族元素A、B形成AB3型分子,下列有关叙述正确的是( )
| A、若A、B为同一周期元素,则AB3分子一定为平面正三角形 |
| B、若AB3分子中的价电子个数为24个,则AB3分子为平面正三角形 |
| C、若为A、B为同一主族元素,则AB3分子一定为三角锥形 |
| D、若AB3分子为三角锥形,则AB3分子一定为NH3 |
 科学家合成了一系列独特的氢铝化合物.最简单的氢铝化合物化学式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )
科学家合成了一系列独特的氢铝化合物.最简单的氢铝化合物化学式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )| A、Al2H6中Al为-3价,H为+l价 |
| B、Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C、Al2H6是共价化合物 |
| D、氢铝化合物可能成为未来的储氢材料和火箭燃料 |
要使氯化铝中的Al3+完全转化为氢氧化铝沉淀,应选用的最佳试剂是( )
| A、硫酸 | B、氨水 |
| C、盐酸 | D、氢氧化钠 |
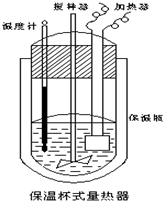 在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.
在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1. 如图中A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物.请回答下列问题:
如图中A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物.请回答下列问题: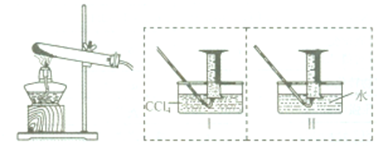
 某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等.已知碳酸锰难溶于水.一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:
某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等.已知碳酸锰难溶于水.一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下: