题目内容
下列说法正确的是( )
| A、1molO2所占体积约为22.4L |
| B、22gCO2中含有的原子数约为6.02×1023 |
| C、100mL0.5mol/LKCl溶液中含溶质的质量为0.05g |
| D、标准状况下,11.2LN2和H2的混合气体所含分子数约为3.01×1023 |
考点:物质的量的相关计算
专题:计算题
分析:A.物质的量一定,温度、压强会影响气体的体积;
B.根据n=
计算二氧化碳的物质的量,再根据N=nNA计算含有原子数目;
C.根据n=cV计算n(KCl),再根据m=nM计算KCl的质量;
D.根据n=
计算混合气体物质的量,再根据N=nNA计算含有分子数目.
B.根据n=
| m |
| M |
C.根据n=cV计算n(KCl),再根据m=nM计算KCl的质量;
D.根据n=
| V |
| Vm |
解答:
解:A.若为标况下,1molO2所占体积约为22.4L,但氧气的温度、压强不确定,其体积不一定为22.4L,故A错误;
B.22g二氧化碳的物质的量为
=0.5mol,含有原子数目为0.5mol×3×6.02×1023mol-1=1.5×6.02×1023,故B错误;
C.n(KCl)=0.1L×0.5mol/L=0.05mol,KCl的质量为0.05mol×74.5g/mol=3.725g,故C错误;
D.混合气体物质的量为
=0.5mol,含有分子数目为0.5mol×6.02×1023mol-1=3.01×1023,故D正确,
故选D.
B.22g二氧化碳的物质的量为
| 22g |
| 44g/mol |
C.n(KCl)=0.1L×0.5mol/L=0.05mol,KCl的质量为0.05mol×74.5g/mol=3.725g,故C错误;
D.混合气体物质的量为
| 11.2L |
| 22.4L/mol |
故选D.
点评:本题考查物质的量有关计算,注意根据PV=nRT理解温度、压强对气体摩尔体积的影响.

练习册系列答案
相关题目
下列物质中互为同分异构体的是( )
| A、O2和O3 |
B、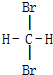 和 和 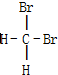 |
| C、CH3COOH和HCOOCH3 |
D、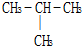 和 和 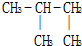 |
下列各组离子中,在溶液中能大量共存的是( )
| A、H+,OH-,Na+,SO42- |
| B、Fe3+,Cl-,K+,I- |
| C、Cu2+,NO3-,Na+,Cl- |
| D、Ba2+,Cl-,K+,CO32- |
25℃、101kPa下,1mol氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O(1)△H=-285.8kJ/mol |
| B、2H2(g)+O2(g)=2H2O(1)△H=+571.6 kJ/mol |
| C、2H2(g)+O2(g)=2H2O(g)△H=-571.6 kJ/mol |
| D、H2(g)+O2(g)=H2O(1)△H=-285.8kJ/mol |
下列各物质中所含原子个数由大到小的顺序排列正确的是( )
(1)0.5mol NH3(2)1mol Ne (3)9g H2O (4)0.2mol H3PO4.
(1)0.5mol NH3(2)1mol Ne (3)9g H2O (4)0.2mol H3PO4.
| A、(1)(4)(3)(2) |
| B、(4)(3)(2)(1) |
| C、(2)(3)(4)(1) |
| D、(1)(4)(2)(3) |
下列说法正确的是( )
| A、共价化合物中可能含有离子键 |
| B、区别离子化合物和共价化合物的方法是看其水溶液是否能够导电 |
| C、离子化合物中只含有离子键 |
| D、离子化合物熔融状态能电离出自由移动的离子,而共价化合物不能 |
对于重水D2O,在25℃时KW=10-12,定义pD=-lg{c(D+)},pOD=-lg{c(OD-)}.则下列说法正确的是( )
| A、25℃时,纯重水pD=7 |
| B、25℃时,0.1mol/L NaCl的重水溶液pD=pOD=6 |
| C、25℃时,1mol/L的DCl的重水溶液pD=0,pOD=14 |
| D、25℃时,0.01mol/L NaOD的重水溶液中pD=12 |