题目内容
16.室温下,下列粒子一定能大量共存的是( )| A. | 使酚酞变红色的溶液:Na+、Fe3+、SO42-、Cl- | |
| B. | 饱和氯水:K+、Na+、Cl-、HSO3- | |
| C. | pH=13溶液:Na+、K+、SiO32-、Cl- | |
| D. | 1.0mol/L KNO3溶液:H+、Fe2+、Cl-、SO32- |
分析 A.使酚酞变红色的溶液,显碱性;
B.饱和氯水含氧化性物质;
C.pH=13溶液,显碱性;
D.离子之间发生氧化还原反应.
解答 解:A.使酚酞变红色的溶液,显碱性,不能大量存在Fe3+,故A错误;
B.饱和氯水含氧化性物质,不能大量存在还原性离子HSO3-,故B错误;
C.pH=13溶液,显碱性,该组离子之间不反应,可大量共存,故C正确;
D.H+、Fe2+、NO3-发生氧化还原反应,H+、NO3-、SO32-发生氧化还原反应,不能共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
4.下列说法错误的是( )
| A. | 金属甲比金属乙容易失去电子,则甲比乙金属性强 | |
| B. | NaHCO3与NaOH反应有CO2生成 | |
| C. | 稀硝酸能将亚铁离子氧化为铁离子 | |
| D. | Na2CO3不能用于治疗胃酸过多 |
1.短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最高的元素,Y是同周期中原子半径最大的元素,Z的最高氧化物的水化物能分别与Y和W的最高氧化的水化物反应生成盐和水,X与W同主族.下列说法不正确的是( )
| A. | X与Y只能形成一种化合物 | |
| B. | 原子半径:r(W)<r(Z)<r(Y) | |
| C. | X的简单气态氢化物的热稳定性比W的强 | |
| D. | Z的最高价氧化物对应的水化物具有两性 |
8.分类法在化学学科发展中起到了非常重要的作用,下列分类标准合理的是( )
| A. | 根据是否含有氧元素,将物质分为氧化剂和还原剂 | |
| B. | 根据是否具有丁达尔现象,将分散系分为溶液、胶体和浊液 | |
| C. | 根据水溶液是否能够导电,将物质分为电解质和非电解质 | |
| D. | 根据反应前后是否有元素化合价变化,可将化学反应分为氧化还原反应和非氧化还原反应 |
5.室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=12的溶液中:AlO2-、Na+、SO42-、SO32- | |
| B. | 水电离出的c(H+)=1×10-12 mol•L-1的溶液中:K+、Na+、SO42-、AlO2- | |
| C. | 加入甲基橙呈黄色的溶液:NH4+、Fe2+、Cl-、NO3- | |
| D. | c(H+)=0.10 mol•L-1的溶液中:CH3COO-、NH4+、Cl-、Na+ |
6.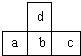 如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )
如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )
 如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )
如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )| A. | a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a | |
| B. | d的氢化物比b的氢化物稳定 | |
| C. | d与c不能形成化合物 | |
| D. | 原子半径的大小顺序是a>b>c>d |