题目内容
11.1g葡萄糖完全氧化,放出约15.6kJ的能量,那么1mol 葡萄糖完全氧化,放出的能量是2808 kJ.化学方程式为C6H12O6+6O2→6CO2+6H2O.分析 1g葡萄糖完全氧化,放出约15.6kJ的能量,所以1mol葡萄糖完全氧化,放出的能量是15.6kJ×180=2808kJ,葡萄糖完全氧化生成二氧化碳和水,由此书写反应的化学方程式.
解答 解:1g葡萄糖完全氧化,放出约15.6kJ的能量,所以1mol葡萄糖完全氧化,放出的能量是15.6kJ×180=2808kJ,葡萄糖完全氧化生成二氧化碳和水,反应的化学方程式为C6H12O6+6O2→6CO2+6H2O;故答案为:2808;C6H12O6+6O2→6CO2+6H2O.
点评 本题考查了化学方程式的书写和热量的相关计算,化学方程式的计算应用,题目较简单.

练习册系列答案
相关题目
2.将100mL 4mol/L Cu(NO3)2溶液电解一段时间(用碳电极),在阳极收集到1.12L气体.将电解后溶液中加入铁粉,最多溶解的铁粉质量为(设反应前后溶液体积不变)( )
| A. | 16.8g | B. | 22.4g | C. | 21g | D. | 19.6g |
19.有关钴和铁化合物的性质见下表.用含钴废料(含少量铁)可制备氯化钴:Co+2HCl═CoCl2+H2↑,工艺流程如下,试回答:
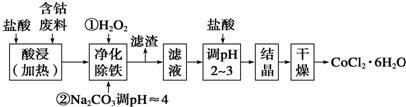
(1)钢铁在潮湿的空气中发生吸氧腐蚀的正极反应式为O2+4e-+2H2O=4OH-.
(2)生铁中含有一种铁碳化合物X(Fe3C).X在足量的空气中高温煅烧,生成有磁性的固体Y,Y可溶于过量盐酸,形成黄绿色的溶液,写出Y与盐酸反应的化学方程式Fe3O4+8HCl=2FeCl3+FeCl2+4H2O.
(3)“净化除铁”中,写出加入H2O2时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)滤液的主要成分是CoCl2、NaCl、HCl.
(5)②步中用Na2CO3调pH≈4的原因是碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全.

| 物质 | 溶度积Ksp | 沉淀完全时的pH |
| Co(OH)2 | 5.9×10-15 | 9.4 |
| Fe(OH)2 | 1.6×10-14 | 9.6 |
| Fe(OH)3 | 1.1×10-36 | 3.7 |
(2)生铁中含有一种铁碳化合物X(Fe3C).X在足量的空气中高温煅烧,生成有磁性的固体Y,Y可溶于过量盐酸,形成黄绿色的溶液,写出Y与盐酸反应的化学方程式Fe3O4+8HCl=2FeCl3+FeCl2+4H2O.
(3)“净化除铁”中,写出加入H2O2时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)滤液的主要成分是CoCl2、NaCl、HCl.
(5)②步中用Na2CO3调pH≈4的原因是碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全.
6.下列关于食品添加剂的叙述中不正确的是( )
| A. | 醋可同时用作防腐剂和调味剂 | |
| B. | 亚硝酸钠可以用作防腐剂,但不宜过量 | |
| C. | 我国应禁止使用味精 | |
| D. | 绝大多数食品添加剂在过量使用时对人体有害的 |
16. 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
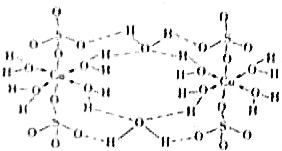
下列说法正确的是( )| A. | 在如图结构示意图中,所有氧原子都采用sp3杂化 | |
| B. | 在如图结构示意图中,存在配位键、共价键和离子键 | |
| C. | 胆矾是分子晶体,分子间存在氢键 | |
| D. | 胆矾中的水在不同温度下会分步失去 |
3.在一定温度下,对可逆反应A(g)+3B(g)?3C(g)的下列叙述中,能说明反应已达到平衡的是( )
| A. | C生成的速率与C分解的速率相等 | |
| B. | 单位时间内消耗amolA和同时生成3amolC | |
| C. | 容器内的压强不再变化 | |
| D. | 混合气体的总物质的量不再变化 |
16.室温下,下列粒子一定能大量共存的是( )
| A. | 使酚酞变红色的溶液:Na+、Fe3+、SO42-、Cl- | |
| B. | 饱和氯水:K+、Na+、Cl-、HSO3- | |
| C. | pH=13溶液:Na+、K+、SiO32-、Cl- | |
| D. | 1.0mol/L KNO3溶液:H+、Fe2+、Cl-、SO32- |
17.勒沙特列原理是自然界一条重要的基本原理.下列事实不能用勒沙特列原理解释的是( )
| A. | NO2气体受压缩后,颜色先变深后变浅 | |
| B. | 对2HI(g)?H2(g)+I2(g)平衡体系加压,颜色迅速变深 | |
| C. | 合成氨工业采用高温、高压工艺提高氨的产率 | |
| D. | 配制硫酸亚铁溶液时,常加入少量铁屑防止氧化 |