题目内容
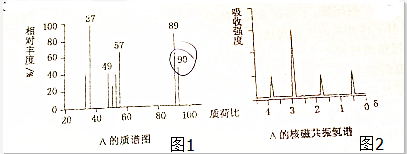
人体摄入的淀粉会水解为葡萄糖,葡萄糖在一定条件下转化成有机物A,A中的碳、氢、氧的质量分数分别为40%、6.7%、53.3%;A的质谱图和核磁共振氢谱如图1、图2所示;已知0.45gA与0.20mol/L 的NaOH溶液25mL恰好完全反应;A和浓硫酸共热,可生成六元环状化合物B.
(1)葡萄糖的结构简式为 ;
(2)有机物A的实验式为 ;
(3)A与足量NaOH 溶液反应的化学方程式为 .
(4)B的结构简式为 ;
(5)A的同分异构体中含有酯基的结构有 种,任写其中一种结构简式为 .

(1)葡萄糖的结构简式为
(2)有机物A的实验式为
(3)A与足量NaOH 溶液反应的化学方程式为
(4)B的结构简式为
(5)A的同分异构体中含有酯基的结构有
考点:有机物实验式和分子式的确定,有机物的推断
专题:
分析:A中的碳、氢、氧的质量分数分别为40%、6.7%、53.5%,则N(C):N(H):N(O)=
:
:
=1:2:1,故A的实验为CH2O,由A的质谱图可知,其相对分子质量为90,设A的分子式为(CH2O)x,则30x=90,故x=3,则A的分子式为C3H6O3,由核磁共振氢谱可知,分子中含有4种氢原子,0.45gA为
=0.005mol,n(NaOH)=0.025L×0.2mol/L=0.005mol,二者恰好完全反应,则A含有1个-COOH,A和浓硫酸共热,可生成六元环状化合物B,A中应含有羟基,且-OH与-COOH连在同一碳原子上,故A的结构简式为 ,B为
,B为 ,据此解答.
,据此解答.
| 40% |
| 12 |
| 6.7% |
| 1 |
| 53.3% |
| 16 |
| 0.45g |
| 90g/mol |
 ,B为
,B为 ,据此解答.
,据此解答.解答:
解:A中的碳、氢、氧的质量分数分别为40%、6.7%、53.5%,则N(C):N(H):N(O)=
:
:
=1:2:1,故A的实验为CH2O,由A的质谱图可知,其相对分子质量为90,设A的分子式为(CH2O)x,则30x=90,故x=3,则A的分子式为C3H6O3,由核磁共振氢谱可知,分子中含有4种氢原子,0.45gA为
=0.005mol,n(NaOH)=0.025L×0.2mol/L=0.005mol,二者恰好完全反应,则A含有1个-COOH,A和浓硫酸共热,可生成六元环状化合物B,A中应含有羟基,且-OH与-COOH连在同一碳原子上,故A的结构简式为 ,B为
,B为 ,
,
(1)葡萄糖的结构简式为:HOCH2(CHOH)4CHO,故答案为:HOCH2(CHOH)4CHO;
(2)由上述分析可知,有机物A的实验式为CH2O,故答案为:CH2O;
(3)A与足量NaOH 溶液反应的化学方程式为 +NaOH→
+NaOH→ +H2O,故答案为:
+H2O,故答案为: +NaOH→
+NaOH→ +H2O;
+H2O;
(4)由上述分析可知,B的结构简式为 ,故答案为:
,故答案为: ;
;
(5)A的同分异构体中含有酯基,符合条件的同分异构体有:HOCH2CH2OOCH,CH3CH(OH)OOCH,CH3CH2OOCOH,HOCH2OOCCH3,CH3OOCCH2OH,共有5种,
故答案为:5;HOCH2CH2OOCH等.
| 40% |
| 12 |
| 6.7% |
| 1 |
| 53.3% |
| 16 |
| 0.45g |
| 90g/mol |
 ,B为
,B为 ,
,(1)葡萄糖的结构简式为:HOCH2(CHOH)4CHO,故答案为:HOCH2(CHOH)4CHO;
(2)由上述分析可知,有机物A的实验式为CH2O,故答案为:CH2O;
(3)A与足量NaOH 溶液反应的化学方程式为
 +NaOH→
+NaOH→ +H2O,故答案为:
+H2O,故答案为: +NaOH→
+NaOH→ +H2O;
+H2O;(4)由上述分析可知,B的结构简式为
 ,故答案为:
,故答案为: ;
;(5)A的同分异构体中含有酯基,符合条件的同分异构体有:HOCH2CH2OOCH,CH3CH(OH)OOCH,CH3CH2OOCOH,HOCH2OOCCH3,CH3OOCCH2OH,共有5种,
故答案为:5;HOCH2CH2OOCH等.
点评:本题考查有机物推断、同分异构体书写、有机反应方程式书写等,计算确定有机物分子式是关键,(5)中同分异构体的书写为易错点、难点,学生容易忽略碳酸与醇形成的酯.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
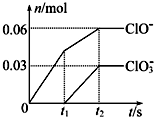 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、反应中转移电子的物质的量是0.21 mol |
| B、ClO3-的生成是由于温度升高引起的 |
| C、苛性钾溶液中KOH的质量为5.04g |
| D、反应中氧化剂和还原剂的物质的量之比为7:3 |
根据表中提供的数据判断下列说法不正确的是( )
| 化学式 | 电离常数(25℃) |
| HCN | K=5.0×10-10 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
| A、等浓度等体积的NaCN、NaHCO3溶液混合:c(Na+)+c(H+)=c(HCO3-)+c(CN-)+c(OH-)+2c(CO32-) | ||
B、若NaCN的水解平衡常数为:Kh=
| ||
| C、等浓度等体积的NaCN和NaCl溶液中离子数目前者大于后者 | ||
| D、过量CO2通入NaCN溶液中:CO2+H2O+CN-=HCO3-+HCN |
下列叙述正确的是( )
| A、向海水中加碱、过滤、加酸,之后浓缩结晶、过滤、干燥、电解能得到金属镁 |
| B、将淡黄色的过氧化钠粉末加入到石蕊试液中,石蕊试液先变红后褪色 |
| C、合金性能一般优于纯金属,钢铁比纯铁具有更好的抗锈蚀能力 |
| D、将碘水倒入分液漏斗,加适量乙醇振荡后静置,可将碘萃取到乙醇中 |
下列说法不正确的是( )
| A、NaOH属于强电解质是因为其可以完全电离 |
| B、电解质溶液可以导电是因为溶液中存在自由移动的离子 |
| C、工业上用电解熔融的氯化铝来制备金属铝 |
| D、碳酸钠溶液与澄清石灰水反应的离子方程式可表示为:Ca2++CO32-=CaCO3↓ |



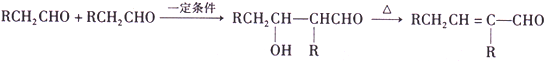
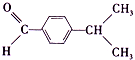 )合成兔耳草醛的路线如下:
)合成兔耳草醛的路线如下: