题目内容
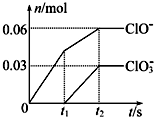 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、反应中转移电子的物质的量是0.21 mol |
| B、ClO3-的生成是由于温度升高引起的 |
| C、苛性钾溶液中KOH的质量为5.04g |
| D、反应中氧化剂和还原剂的物质的量之比为7:3 |
考点:离子方程式的有关计算
专题:
分析:A.氯气和氢氧化钾溶液反应生成次氯酸钾、氯化价和氯酸钾,根据图象知n(ClO-)=0.06mol,n(ClO3-)=0.03mol,由ClO-、ClO3-的物质的量,结合Cl元素化合价变化计算转移电子数目;
B.根据图象知,氯气和氢氧化钾先生成次氯酸钾,且该反应是放热反应,随着温度的升高,氯气和氢氧化钾反应生成氯酸钾;
C.根据电子转移守恒计算n(Cl-),根据物料守恒可知n(K+)=n(Cl-)+n(ClO-)+n(ClO3-),结合m=nM计算KOH质量;
D.在反应中Cl2既做氧化剂又做还原剂,做氧化剂的Cl2被还原为Cl-,做还原剂的Cl2被氧化为ClO-和ClO3-,据此分析.
B.根据图象知,氯气和氢氧化钾先生成次氯酸钾,且该反应是放热反应,随着温度的升高,氯气和氢氧化钾反应生成氯酸钾;
C.根据电子转移守恒计算n(Cl-),根据物料守恒可知n(K+)=n(Cl-)+n(ClO-)+n(ClO3-),结合m=nM计算KOH质量;
D.在反应中Cl2既做氧化剂又做还原剂,做氧化剂的Cl2被还原为Cl-,做还原剂的Cl2被氧化为ClO-和ClO3-,据此分析.
解答:
解:A.氯气和氢氧化钠溶液反应生成次氯酸钠、氯化钠和氯酸钠,根据图象知n(ClO-)=0.06mol,n(ClO3-)=0.03mol,故转移电子物质的量=0.06mol×(1-0)+0.03mol×(5-0)=0.21mol,故A正确;
B.根据图象知,氯气和氢氧化钾先生成次氯酸钾,且该反应是放热反应,随着温度的升高,氯气和氢氧化钾反应生成氯酸钾,所以氯酸根离子的生成是由于温度升高引起的,故B正确;
C.根据电子转移守恒可知n(Cl-)=0.21mol,根据物料守恒可知n(K+)=n(Cl-)+n(ClO-)+n(ClO3-)=0.21mol+0.06mol+0.03mol=0.3mol,则n(KOH)=0.3mol,则氢氧化钾质量=0.3mol×56g/mol=16.8g,故C错误;
D.在反应中Cl2既做氧化剂又做还原剂,做氧化剂的Cl2被还原为Cl-,做还原剂的Cl2被氧化为ClO-和ClO3-,据氯原子的守恒可知,氧化剂和还原剂的物质的量之比为0.21mol:(0.06+0.03)mol=7:3,故D正确;
故选C.
B.根据图象知,氯气和氢氧化钾先生成次氯酸钾,且该反应是放热反应,随着温度的升高,氯气和氢氧化钾反应生成氯酸钾,所以氯酸根离子的生成是由于温度升高引起的,故B正确;
C.根据电子转移守恒可知n(Cl-)=0.21mol,根据物料守恒可知n(K+)=n(Cl-)+n(ClO-)+n(ClO3-)=0.21mol+0.06mol+0.03mol=0.3mol,则n(KOH)=0.3mol,则氢氧化钾质量=0.3mol×56g/mol=16.8g,故C错误;
D.在反应中Cl2既做氧化剂又做还原剂,做氧化剂的Cl2被还原为Cl-,做还原剂的Cl2被氧化为ClO-和ClO3-,据氯原子的守恒可知,氧化剂和还原剂的物质的量之比为0.21mol:(0.06+0.03)mol=7:3,故D正确;
故选C.
点评:本题考查氧化还原反应的计算,注意根据原子守恒、转移电子守恒来分析解答,题目难度中等.

练习册系列答案
相关题目
有一支50mL酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处.把滴定管中的溶液全部排出,其体积( )
| A、大于40. 00 mL |
| B、等于40.00 mL |
| C、大于10.00 mL |
| D、等于10.00 mL |
下列实验操作要用到玻璃棒的是( )
①溶解 ②过滤 ③蒸发 ④向容量瓶转移液体 ⑤蒸馏 ⑥分液.
①溶解 ②过滤 ③蒸发 ④向容量瓶转移液体 ⑤蒸馏 ⑥分液.
| A、全部 | B、②③④⑤ |
| C、①②③④ | D、①③④⑤⑥ |
某烷烃一个分子里含有9个碳原子,其一氯代物只有两种,这种烷烃的名称是( )
| A、正壬烷 |
| B、2,6二甲基庚烷 |
| C、2,3,4三甲基己烷 |
| D、2,2,4,4四甲基戊烷 |
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1mol氢气的化学键消耗的能量为Q1kJ,破坏1mol氯气的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ,下列关系式正确的是( )
| A、Q1+Q 3 |
| B、Q1+Q2>2Q3 |
| C、Q1+Q2<Q3 |
| D、Q1+Q2<2Q3 |
 ,
,
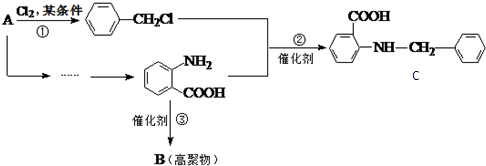

 中官能团的名称
中官能团的名称 多一个碳的同系物,则满足下列条件的D的同分异构体共有
多一个碳的同系物,则满足下列条件的D的同分异构体共有