题目内容
为测定NaOH溶液的浓度,实验如下:用标准稀盐酸溶液进行滴定
(1)配制100mL 0.1000mol?L-1盐酸标准溶液所需仪器除量筒、小烧杯、玻璃棒、胶头滴管外,还需要 .
(2)用 量取20.00mL待测NaOH溶液放入锥形瓶中,滴加2滴~3滴酚酞作指示剂,用标准盐酸溶液进行滴定.
(3)滴定时边滴边摇动锥形瓶,眼睛 .
(4)下列操作会造成测定结果(待测NaOH溶液浓度值)偏低的有 .
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用标准稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数.
(1)配制100mL 0.1000mol?L-1盐酸标准溶液所需仪器除量筒、小烧杯、玻璃棒、胶头滴管外,还需要
(2)用
(3)滴定时边滴边摇动锥形瓶,眼睛
(4)下列操作会造成测定结果(待测NaOH溶液浓度值)偏低的有
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用标准稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数.
考点:中和滴定
专题:实验题
分析:(1)配制100mL0.1000mol/L的盐酸,需要的仪器有量筒、小烧杯、玻璃棒、胶头滴管、100mL的容量瓶;
(2)用碱式滴定管氯气20.00mLNaOH溶液;
(3)滴定时眼睛应注视锥形瓶中溶液颜色变化;
(4)分析错误操作导致V(标准)的变化,据c(待测)=
分析.
(2)用碱式滴定管氯气20.00mLNaOH溶液;
(3)滴定时眼睛应注视锥形瓶中溶液颜色变化;
(4)分析错误操作导致V(标准)的变化,据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
解答:
解:(1)配制100mL0.1000mol/L的盐酸,需要的仪器有量筒、小烧杯、玻璃棒、胶头滴管、100mL的容量瓶,故答案为:100mL的容量瓶;
(2)用碱式滴定管氯气20.00mLNaOH溶液,故答案为:碱式滴定管;
(3)滴定时眼睛应注视锥形瓶中溶液颜色变化,故答案为:滴定管中溶液颜色变化;
(4)A.配制标准溶液定容时,加水超过刻度,导致c(标准)减小,V(标准)增大,据据c(待测)=
分析,c(标准)偏高,故A错误;
B.锥形瓶水洗后直接装待测液,对测定结果无影响,故B错误;
C.酸式滴定管水洗后未用标准稀盐酸溶液润洗,导致c(标准)减小,V(标准)增大,据据c(待测)=
分析,c(标准)偏高,故C错误;
D.滴定到达终点时,俯视读出滴定管读数,导致V(标准)减小,据据c(待测)=
分析,c(标准)偏低,故D正确;
故答案为:D.
(2)用碱式滴定管氯气20.00mLNaOH溶液,故答案为:碱式滴定管;
(3)滴定时眼睛应注视锥形瓶中溶液颜色变化,故答案为:滴定管中溶液颜色变化;
(4)A.配制标准溶液定容时,加水超过刻度,导致c(标准)减小,V(标准)增大,据据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
B.锥形瓶水洗后直接装待测液,对测定结果无影响,故B错误;
C.酸式滴定管水洗后未用标准稀盐酸溶液润洗,导致c(标准)减小,V(标准)增大,据据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
D.滴定到达终点时,俯视读出滴定管读数,导致V(标准)减小,据据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
故答案为:D.
点评:本题考查了配制一定物质的量浓度的溶液所需要的仪器、滴定管使用、中和滴定中的误差分析,注意据据c(待测)=
分析误差,题目难度中等.
| c(标准)×V(标准) |
| V(待测) |

练习册系列答案
相关题目
下列各组离子在溶液中能大量共存的是( )
| A、H+、Cl-、CH3COO-、NO3- |
| B、K+、AlO2-、NO3-、OH- |
| C、Fe3+、I-、SO42-、H+ |
| D、AlO2-、HCO3-、Na+、K+ |
在实验室中,从碘水中提取碘的操作,正确的是( )
| A、分液、蒸馏 |
| B、溶解、过滤、蒸发 |
| C、萃取、分液 |
| D、萃取、分液、蒸馏 |
下列有关物质的性质与其应用不相对应的是( )
| A、Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品 |
| B、NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂 |
| C、晶体硅是半导体材料,可用于计算机芯片的基底 |
| D、K2FeO4能与水作用生成Fe(OH)3胶体和O2,可用于自来水的净化和杀菌消毒 |
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X不可能是( )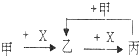

| A、甲:Fe、X:Cl2 |
| B、甲:SO2、X:NaOH溶液 |
| C、甲:C、X:O2 |
| D、甲:AlCl3溶液、X:NaOH溶液 |