题目内容
 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.(1)①用
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V |  |  | 见① |
| 2 | V | 0.50 | 30.8 | 30.30 |
| 3 | V | 6.00 | 36.35 | 30.35 |
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前尖嘴有气泡,滴定结束时气泡消失,则会使测定结果
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果
考点:中和滴定
专题:实验题
分析:(1)①根据酸性溶液存放在酸式滴定管中;根据滴定管的结构以及测量体积的原理来分析;
(2)先考虑数据的合理性,然后求体积的平均值,最后根据c(待测)=
计算;
(3)根据c(待测)=
分析不当操作对V(标准)的影响,以此判断浓度的误差.
(2)先考虑数据的合理性,然后求体积的平均值,最后根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
(3)根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
解答:
解:(1)①盐酸是酸性溶液,存放在酸式滴定管中;滴定前读数为:0.40mL,滴定后读数为:24.90mL,消耗溶液的体积为24.50mL,故答案为:酸;24.50;
(2)3次消耗的盐酸标准液的体积分别为:24.50mL、30.30mL、30.35mL,第1组数据舍去,则平均体积为30.30mL,c(待测)=
=
;
故答案为:
;
(3)a.若滴定前尖嘴有气泡,滴定结束时气泡消失,造成V(标准)偏大,根据c(待测)=
分析,可知c(标准)偏高;
b.读数时,若滴定前仰视,滴定后俯视,造成V(标准)偏小,根据c(待测)=
分析,可知c(标准)偏低;
故答案为:偏高;偏低.
(2)3次消耗的盐酸标准液的体积分别为:24.50mL、30.30mL、30.35mL,第1组数据舍去,则平均体积为30.30mL,c(待测)=
| V(标准)×c(标准) |
| V(待测) |
| 30.30mL×cmol/L |
| VmL |
故答案为:
| 30.30mL×cmol/L |
| VmL |
(3)a.若滴定前尖嘴有气泡,滴定结束时气泡消失,造成V(标准)偏大,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
b.读数时,若滴定前仰视,滴定后俯视,造成V(标准)偏小,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
故答案为:偏高;偏低.
点评:本题主要考查了中和滴定操作、化学计算以及注意事项,难度不大,分析误差时要看是否影响标准体积的用量,若标准体积偏大,结果偏高;若标准体积偏小,则结果偏小;若不影响标准体积,则结果无影响.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有机物中含有两种官能团的是( )
| A、CH2═CHCl |
B、 |
| C、CH2Cl-CH2-CH2Cl |
D、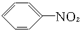 |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、0.1mol?L-1Mg(NO3)2溶液中含有0.2nA个NO3- |
| B、8g CH4中含有10nA个电子 |
| C、常温常压下,22.4L O3中含有3nA个氧原子 |
| D、28g C2H4中含有2nA个碳原子 |
氯化硼的熔点为107℃.在氯化硼分子中,氯硼键之间的夹角为120°,它可水解,水解产物之一能在空气中产生白雾.下列关于氯化硼的说法正确的是( )
| A、氯化硼是原子晶体 |
| B、氯化硼分子是极性分子 |
| C、熔化时,氯化硼能导电 |
| D、水解方程式:BCl3+3H2O=H3BO3+3HCl |
下列物质属于纯净物的是( )
| A、漂白粉 | B、盐酸 | C、氯水 | D、液溴 |
下列有关中和滴定的操作:①用标准液润洗滴定管;②往滴定管内注入标准溶液;③检查滴定管是否漏水;④滴定;⑤滴加指示剂于待测液中;⑥调节液面处于某一刻度.正确的操作顺序是( )
| A、③①②⑥⑤④ |
| B、⑤①②⑥④③ |
| C、⑤④③②①⑥ |
| D、③①②④⑤⑥ |
将CO2和C加入密闭容器中,在一定条件下发生反应:CO2(g)+C(s)?2CO(g),忽略固体体积,平衡时CO的体积分数(%)随温度和压强的变化如下表所示:
下列判断不正确的是( )
| 温度/℃ CO的体积分数/% 压强/MPa | 1.0 | 2.0 | 3.0 |
| 800 | 54.0 | a | b |
| 900 | c | 75.0 | d |
| 1000 | e | f | 80.0 |
| A、b<f |
| B、900℃,2.0MPa的转化率为60% |
| C、K(1000℃)=3.2 |
| D、K(1000℃)>K(800℃) |