题目内容
7.M是一种新型可生物降解的高分子材料,主要制造可降解纤维、塑料和医用材料,其水解最终产物为N.燃烧9.0g的N只产生CO2和H2O,且质量分别为13.2g和5.4g,实验测得N在标准状况下的蒸气密度为4.02g/L;N的核磁共振氢谱显示的峰面积之比为1:1:1:3.(1)通过计算确定N的分子式
(2)写出N的结构简式,并写出N在催化剂条件下缩聚反应合成M的化学方程式.
分析 由密度可确定有机物的相对分子质量,进而计算9.0g有机物的物质的量,计算生成二氧化碳、水的物质的量,确定1mol有机物含有C、H、O的个数,可确定有机物分子式,结合性质确定有机物结构简式,以此解答该题.
解答 解:(1)M(N)=4.02g/L×22.4L/mol=90g/mol,n(N)=$\frac{9.0g}{90g/mol}$=0.1mol/L,
1molN中:n(C)=$\frac{13.2g}{44g/mol}$÷0.1mol=3mol;
n(H)=$\frac{5.4g}{18g/mol}×2$÷0.1mol=6mol;
n(O)=(90-12×3-1×6)÷16=3(mol),
则有机物的分子式为C3H6O3,
答:N的分子式为C3H6O3;
(2)N在催化剂条件下缩聚反应合成M,可知N为 ,M为
,M为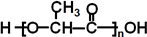 ,反应的方程式为
,反应的方程式为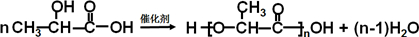 ,
,
答: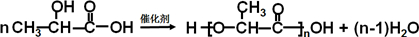 .
.
点评 本题考查了有机物的计算与推断,为高考常见题型,侧重于学生的分析、计算能力的考查,答题时注意O元素的确定,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.苹果酸( )易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )
)易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )
 )易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )
)易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )| A. | 苹果酸属于烃 | B. | 苹果酸中有3种官能团 | ||
| C. | 苹果酸的分子式是C3H6O5 | D. | 苹果酸能使紫色石蕊溶液变红 |
18.下列化学实验事实及其结论都正确的是( )
| A. | 将SO2通入含HClO的溶液中生成H2SO4,酸性:HClO>H2SO4 | |
| B. | 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝熔点高于铝 | |
| C. | SiO2可以和NaOH溶液及HF溶液反应,SiO2属于两性氧化物 | |
| D. | SO2使溴水褪色,SO2具有漂白性 |
15.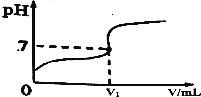 常温下,用0.2000mol/L的MOH溶液滴定10mL同浓度的一元弱酸HA,滴定过程溶液pH随MOH溶液V的变化曲线如图所示HCl溶液,滴定曲线如图所示(忽略中和热效应),下列说法不正确的是( )
常温下,用0.2000mol/L的MOH溶液滴定10mL同浓度的一元弱酸HA,滴定过程溶液pH随MOH溶液V的变化曲线如图所示HCl溶液,滴定曲线如图所示(忽略中和热效应),下列说法不正确的是( )
 常温下,用0.2000mol/L的MOH溶液滴定10mL同浓度的一元弱酸HA,滴定过程溶液pH随MOH溶液V的变化曲线如图所示HCl溶液,滴定曲线如图所示(忽略中和热效应),下列说法不正确的是( )
常温下,用0.2000mol/L的MOH溶液滴定10mL同浓度的一元弱酸HA,滴定过程溶液pH随MOH溶液V的变化曲线如图所示HCl溶液,滴定曲线如图所示(忽略中和热效应),下列说法不正确的是( )| A. | HA溶液加水稀释后,溶液中$\frac{n(HA)}{n({A}^{-})}$的值减小 | |
| B. | 当V1=10时,MOH一定是弱碱 | |
| C. | 当V1=10时,溶液中水的电离程度最大 | |
| D. | 当V1>10时,溶液中离子浓度关系一定是c(M+)>c(A-)>c(OH-)>c(H+) |
12.乙烯与酸性高锰酸钾反应会放出CO2,下列操作中既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中混有的少量乙烯的操作方法是( )
| A. | 混合气通过盛有水的洗气瓶 | |
| B. | 混合气与过量氢气混合 | |
| C. | 混合气通过装有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 通过装有过量溴水的洗气瓶 |
4.已知丁基有4种结构,则分子式为C5H10O2且能与NaHCO3发生反应的羧酸有( )种.
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
2.将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3mol•L-1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是( )
| A. | 开始加入合金的质量可能为3.6g | |
| B. | 参加反应的硝酸的物质的量为0.1mol | |
| C. | 沉淀完全时消耗NaOH溶液的体积为100mL | |
| D. | 溶解合金时产生NO的体积为2.24L |