题目内容
1.钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀.金属发生电化学腐蚀时,可分为析氢腐蚀和吸氧腐蚀.两者的本质相同,该腐蚀过程中负极电极反应式为Fe-2e-=Fe2+,但正极反应不同,析氢腐蚀的正极反应为2H++2e-=H2↑,钢铁腐蚀主要是吸氧腐蚀,吸氧腐蚀的正极反应为O2+2H2O+4e-=4OH-.分析 析氢腐蚀和吸氧腐蚀的负极均为Fe失去电子,析氢腐蚀的正极反应为氢离子得到电子,吸氧腐蚀的正极反应为氧气得到电子,以此来解答.
解答 解:析氢腐蚀和吸氧腐蚀的本质相同,该腐蚀过程中负极电极反应式为Fe-2e-=Fe2+,但正极反应不同,析氢腐蚀的正极反应为2H++2e-=H2↑,钢铁腐蚀主要是吸氧腐蚀,吸氧腐蚀的正极反应为O2+2H2O+4e-=4OH-,
故答案为:Fe-2e-=Fe2+;2H++2e-=H2↑;O2+2H2O+4e-=4OH-.
点评 本题考查电化学腐蚀,为高频考点,把握原电池原理的应用、电极反应的书写为解答的关键,侧重分析与应用能力的考查,注意正极反应的区别,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.如图所示的锌、铜和稀硫酸组成的原电池,工作时下列说法正确的是( )
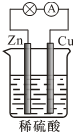

| A. | 反应一段时间后,溶液的酸性减弱 | |
| B. | 电子由Zn经外电路流向Cu,再经硫酸溶液流回Zn | |
| C. | 负极的反应式为2H++2e-═H2↑ | |
| D. | 硫酸作电解质起导电的作用,故浓度保持不变 |
16.将含有O2和CH4的混合气体置于盛有23.4g Na2O2的密闭容器中,电火花点燃,反应结束,容器内的压强为零(温度150℃),将残留物溶于水,无气体产生,下列叙述正确的是( )
| A. | 原混合气体中O2和CH4的体积比为2:1 | |
| B. | 残留物中只有Na2CO3 | |
| C. | 原混合气体中O2和CH4的物质的量之比为1:2 | |
| D. | 残留物只有Na2CO3和NaOH |
10.下列化学用语正确的是( )
| A. | H2O2的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | 次氯酸的结构式:H-O-Cl | |
| C. | S2-的结构示意图: | |
| D. | CO2的比例模型: |
11.下列化学电池不易造成环境污染的是( )
| A. | 铅蓄电池 | B. | 锌锰电池 | C. | 镍镉电池 | D. | 甲烷燃料电池 |
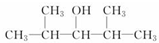 B.
B.
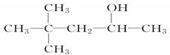 D.CH3(CH2)5CH2OH
D.CH3(CH2)5CH2OH