题目内容
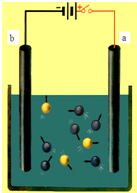 如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )
如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )| A、a为正极,b为负极 |
| B、a极上发生还原反应 |
| C、电解过程中,b电极上有铜析出 |
| D、电解过程中,氯离子浓度保持不变 |
考点:电解原理
专题:电化学专题
分析:电解氯化铜溶液时,连接电源负极的电极是阴极,阴极上铜离子得电子析出铜单质;连接电源正极的电极是阳极,阳极上氯离子失电子生成氯气,据此分析.
解答:
解:A、b连接电源负极,是阴极,a连接电源正极,是阳极,故A错误;
B、a连接电源正极,是阳极,发生氧化反应,故B错误;
C、b连接电源负极,是阴极,电解过程中,b电极上铜离子得电子有铜析出,故C正确;
D、连接电源正极的电极a是阳极,阳极上氯离子失电子生成氯气,电解过程中,氯离子浓度减小,故D错误;
故选C.
B、a连接电源正极,是阳极,发生氧化反应,故B错误;
C、b连接电源负极,是阴极,电解过程中,b电极上铜离子得电子有铜析出,故C正确;
D、连接电源正极的电极a是阳极,阳极上氯离子失电子生成氯气,电解过程中,氯离子浓度减小,故D错误;
故选C.
点评:本题考查了电解池原理,难度不大,明确溶液中离子的放电顺序是解本题的关键.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
下列各组物质的溶液,不另加试剂无法一一鉴别的是( )
| A、NaOH HCl CuSO4 MgSO4 |
| B、Na2CO3 K2SO4 BaCl2 HCl |
| C、KNO3 HCl CaCl2 NaOH |
| D、NH4NO3 H2SO4 NaOH MgCl2 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、24克镁单质变为镁离子时,失去的电子数为NA |
| B、18克水所含的电子数为NA |
| C、8克氦气所含分子数为NA |
| D、3.2克氧气所含氧原子数为0.2NA |
用惰性电极分别电解下列物质的水溶液一段时间后,溶液的pH会升高的是( )
| A、Ba(NO3)2 |
| B、CuSO4 |
| C、HNO3 |
| D、NaOH |
利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是( )
①电解时以精铜作阳极
②电解时阴极发生还原反应
③粗铜连接电源负极,其电极反应是Cu-2e-=Cu2+
④电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥.
①电解时以精铜作阳极
②电解时阴极发生还原反应
③粗铜连接电源负极,其电极反应是Cu-2e-=Cu2+
④电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥.
| A、①② | B、②④ | C、②③ | D、③④ |
下列叙述正确的是( )
| A、电解池的阴极上都是发生失电子的氧化反应 |
| B、用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2 |
| C、用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1molNaOH |
| D、酸、碱、盐溶液电解后pH都增大 |
用铂电极(惰性)电解下列电解质溶液,电解质的浓度增大且溶液的pH不变的是( )
| A、NaOH溶液 |
| B、CuSO4溶液 |
| C、Na2SO4溶液 |
| D、NaCl溶液 |
下列实验设计或实验操作中,正确的是( )
A、铜与浓硝酸反应制NO2:可采用如图装置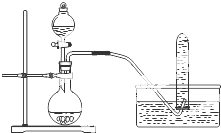 |
| B、分离乙酸和乙醇溶液:用分液漏斗进行分离 |
| C、稀硫酸和锌粒反应制取氢气:加入少许硫酸铜以加快反应速率 |
| D、鉴别Na2CO3溶液和NaHCO3溶液:分别向两种溶液滴加澄清石灰水至过量 |