题目内容
将13.44L(标准状况)乙烯和乙烷的混合气体通入足量的溴的四氯化碳溶液中,充分反应后,溴的四氯化碳溶液的质量增加了5.6g.求原气体混合物中乙烯与乙烷的物质的量之比.
考点:有关混合物反应的计算
专题:计算题
分析:根据乙烯含有双键,能与溴水发生加成反应,乙烷不能与溴水反应,溴水的质量增加了5.6g为乙烯的质量,根据n=
计算乙烯的物质的量,根据n=
计算混合气体物质的量,进而计算乙烷物质的量.
| m |
| M |
| V |
| Vm |
解答:
解:13.44L混合气体的物质的量为
=0.6mol,
乙烯含有双键,能与溴水发生加成反应,乙烷不能与溴水反应,溴水的质量增加了5.6g为乙烯的质量,所以乙烯的物质的量为
=0.2mol,
则乙烷的物质的量为:0.6mol-0.2mol=0.4mol,
所以乙烯与乙烷的物质的量之比为0.2mol:0.4mol=1:2,
答:原气体混合物中乙烯与乙烷的物质的量之比为1:2.
| 13.44L |
| 22.4L/mol |
乙烯含有双键,能与溴水发生加成反应,乙烷不能与溴水反应,溴水的质量增加了5.6g为乙烯的质量,所以乙烯的物质的量为
| 5.6g |
| 28g/mol |
则乙烷的物质的量为:0.6mol-0.2mol=0.4mol,
所以乙烯与乙烷的物质的量之比为0.2mol:0.4mol=1:2,
答:原气体混合物中乙烯与乙烷的物质的量之比为1:2.
点评:本题考查混合物计算,比较基础,侧重考查物质的量的有关计算,注意乙烯与乙烷的性质差别.

练习册系列答案
相关题目
不能鉴别AgNO3、BaCl2、K2SO3和Mg(NO3)2四种溶液(不考虑他们间的相互反应)的试剂组是( )
| A、盐酸、硫酸 |
| B、盐酸、NaOH溶液 |
| C、氨水、硫酸 |
| D、氨水、NaOH溶液 |
据报道,月球的土壤中吸附着数百万吨的 He,每百吨 He核聚变所释放出的能量相当于目前人类一年消耗的能量.地球上氦元素主要以42He的形式存在下列说法正确的是( )
| A、42He原子核内有4个质子 |
| B、42He的最外层电子数为2 |
| C、32He原子核内含有3个质子 |
| D、32He与42He互为同位素 |
下列各组溶液,不用其它试剂,无法将它们区别开的是( )
| A、HCl、CuSO4、Mg(NO3)2、KOH |
| B、NaBr、AgNO3、HCl、Na2CO3 |
| C、H2SO4、NaCl、Na2SO4、Na2CO3 |
| D、NaOH、MgSO4、Na2CO3、KHSO4 |
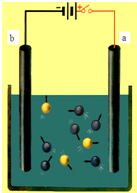 如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )
如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )| A、a为正极,b为负极 |
| B、a极上发生还原反应 |
| C、电解过程中,b电极上有铜析出 |
| D、电解过程中,氯离子浓度保持不变 |
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是( )
| A、NaOH、H2SO4、Na2SO4 |
| B、NaOH、AgNO3、H2SO4 |
| C、HCl、CuBr2、Ba(OH)2 |
| D、KBr、H2SO4、Ba(OH)2 |