题目内容
下列实验设计或实验操作中,正确的是( )
A、铜与浓硝酸反应制NO2:可采用如图装置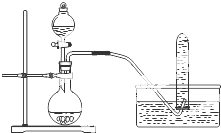 |
| B、分离乙酸和乙醇溶液:用分液漏斗进行分离 |
| C、稀硫酸和锌粒反应制取氢气:加入少许硫酸铜以加快反应速率 |
| D、鉴别Na2CO3溶液和NaHCO3溶液:分别向两种溶液滴加澄清石灰水至过量 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.NO2能与水反应生成一氧化氮;
B.乙醇和乙酸互溶;
C.利用原电池来分析加快反应速率;
D.Na2CO3溶液和NaHCO3溶液均与石灰水反应生成白色沉淀.
B.乙醇和乙酸互溶;
C.利用原电池来分析加快反应速率;
D.Na2CO3溶液和NaHCO3溶液均与石灰水反应生成白色沉淀.
解答:
解:A.NO2能与水反应生成一氧化氮,不能用排水法收集,故A错误;
B.乙醇和乙酸互溶,不能用分液漏斗进行分离,故B错误;
C.加入少许硫酸铜,锌置换出铜,构成锌、铜原电池,从而加快了生成氢气的反应速率,故C正确;
D.Na2CO3溶液和NaHCO3溶液均与石灰水反应生成白色沉淀,现象相同,不能鉴别,故D错误.
故选C.
B.乙醇和乙酸互溶,不能用分液漏斗进行分离,故B错误;
C.加入少许硫酸铜,锌置换出铜,构成锌、铜原电池,从而加快了生成氢气的反应速率,故C正确;
D.Na2CO3溶液和NaHCO3溶液均与石灰水反应生成白色沉淀,现象相同,不能鉴别,故D错误.
故选C.
点评:本题考查物质的制备、分离提纯以及检验,为高频考点,把握物质的性质及发生的反应、反应现象是解答本题的关键,注意物质性质的差异即可解答,题目难度不大.

练习册系列答案
相关题目
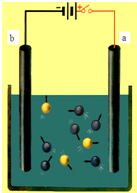 如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )
如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )| A、a为正极,b为负极 |
| B、a极上发生还原反应 |
| C、电解过程中,b电极上有铜析出 |
| D、电解过程中,氯离子浓度保持不变 |
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是( )
| A、NaOH、H2SO4、Na2SO4 |
| B、NaOH、AgNO3、H2SO4 |
| C、HCl、CuBr2、Ba(OH)2 |
| D、KBr、H2SO4、Ba(OH)2 |
有机物X、Y分子式不同,它们只含C、H、O元素中的两种或三种,若将X、Y不论以何种比例混合,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变.X、Y可能是( )
| A、C2H4 与 C3H4O |
| B、C2H2 与 C6H6 |
| C、CH2O 与 C3H6O2 |
| D、CH4 与 C2H4O2 |
下列每组中的两种物质,能用分液漏斗分离的是( )
| A、四氯化碳和水 |
| B、食盐和水 |
| C、食用油和汽油 |
| D、酒精和水 |
在相同条件下,0.1mol镁和0.1mol铝分别和足量的稀盐酸起反应后产生的氢气( )
| A、镁产生的多 |
| B、铝产生的多 |
| C、镁和铝产生的一样多 |
| D、无法比较 |