题目内容
已知有如下氧化还原反应:Zn+2HNO3+NH4NO3=N2↑+Zn(NO3)2+3H2O,则:
(1)该反应的还原剂为 ,还原产物为 .(写化学式)
(2)若产生的N2在标准状况下体积为2.24L,则反应中转移了 mol电子.
(1)该反应的还原剂为
(2)若产生的N2在标准状况下体积为2.24L,则反应中转移了
考点:氧化还原反应,氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:Zn+2HNO3+NH4NO3=N2↑+Zn(NO3)2+3H2O中,Zn元素的化合价由0升高为+2价,N元素的化合价既升高又降低,以此来解答.
解答:
解:(1)因Zn元素的化合价升高,铵根离子中N元素的化合价升高,则还原剂为Zn和NH4NO3;硝酸中N元素的化合价降低,则N2为还原产物,
故答案为:Zn和NH4NO3;N2;
(2)由反应可知,生成1molN2转移5mol电子,产生的N2在标准状况下体积为2.24L,其物质的量为0.1mol,则转移0.5mol电子,故答案为:0.5.
故答案为:Zn和NH4NO3;N2;
(2)由反应可知,生成1molN2转移5mol电子,产生的N2在标准状况下体积为2.24L,其物质的量为0.1mol,则转移0.5mol电子,故答案为:0.5.
点评:本题考查氧化还原反应,为高考高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念和电子转移的考查,题目难度不大.

练习册系列答案
相关题目
下列能达到实验目的是( )
A、 吸收氨气制氨水 |
B、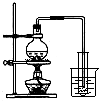 制取少量蒸馏水 |
C、 转移溶液 |
D、 除去杂质气体CO2 |
决定1mol不同气体体积大小的主要因素有( )
①气体分子直径
②气体分子数目
③气体分子间距
④气体分子质量.
①气体分子直径
②气体分子数目
③气体分子间距
④气体分子质量.
| A、①②③ | B、②③ | C、③ | D、③④ |
下列物质的贮存方法错误的是( )
| A、金属钠存放于煤油中 |
| B、硝酸贮存在避光、低温处 |
| C、氯水贮存在棕色瓶中,放在冷暗处 |
| D、烧碱溶液贮存在带玻璃塞的细口瓶中 |
我国所生产的碘盐中含有少量的碘酸钾(KIO3),以补充人体所需的碘元素而预防甲状腺疾病,而核应急专用碘片中含有的主要成分是碘化钾(KI),食用一定的碘片可以阻止放射性碘被人体甲状腺所吸收,那碘化钾中碘元素的化合价为( )
| A、+5 | B、+1 | C、-5 | D、-1 |
以下化学反应的离子方程式书写正确的是( )
| A、硫酸与氢氧化钡溶液反应:H++OH-=H2O |
| B、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| C、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ |
| D、氯气与溴化钠溶液反应:Cl2+2Br-=Br2+2Cl- |
常温下,0.1mol/L Na2CO3溶液中各微粒浓度关系正确的是( )
| A、c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3) |
| B、c(Na+)>c(CO32-)>c(H+)>c(OH-) |
| C、c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| D、c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |