题目内容
下列能达到实验目的是( )
A、 吸收氨气制氨水 |
B、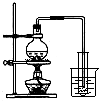 制取少量蒸馏水 |
C、 转移溶液 |
D、 除去杂质气体CO2 |
考点:化学实验方案的评价,物质的分离、提纯和除杂,实验室制取蒸馏水,配制一定物质的量浓度的溶液
专题:实验评价题
分析:A.氨气极易溶于水;
B.蒸馏水中杂质难挥发;
C.转移液体需用玻璃棒引流;
D.洗气长进短出.
B.蒸馏水中杂质难挥发;
C.转移液体需用玻璃棒引流;
D.洗气长进短出.
解答:
解:A.氨气极易溶于水,易发生倒吸,应使漏斗下端与液面相平,故A错误;
B.蒸馏水中杂质难挥发,长导管可起冷凝作用,故B正确;
C.转移液体应用玻璃棒引流,故C错误;
D.洗气长进短出,否则会将液体排出,故D错误.
故选B.
B.蒸馏水中杂质难挥发,长导管可起冷凝作用,故B正确;
C.转移液体应用玻璃棒引流,故C错误;
D.洗气长进短出,否则会将液体排出,故D错误.
故选B.
点评:本题考查化学实验的基本操作,题目难度不大,注意相关基本实验操作的实验注意事项.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
在氧化还原反应中,下列说法正确的是( )
| A、失去电子被氧化,发生了氧化反应,该物质是氧化剂 |
| B、氧化剂被氧化,还原剂被还原 |
| C、氧化剂得到电子被还原,其产物为氧化产物 |
| D、得到电子的物质被还原,元素化合价降低,表现氧化性 |
在无色透明的溶液中可以大量共存的离子组是( )
| A、H+、K+、ClO-、NO3- |
| B、Fe3+ Na+ SCN-、Cl- |
| C、Cu2+、NO3-、OH-、Cl- |
| D、Mg2+、K+、Cl-、NO3- |
下列各组离子中能大量共存的是( )
| A、K+、SiO32-、OH-、Na+ |
| B、Na+、H+、CO32-、SO42- |
| C、K+、H+、SiO32-、Cl- |
| D、OH-、Na+、HCO3-、Cl- |
已知多硫化钠Na2Sx(x≥2)在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,反应中Na2Sx与NaClO的物质的量之比为1:10,则x值是( )
| A、2 | B、3 | C、4 | D、5 |
 常温下,等体积pH值等于2的两种酸溶液HA和HB,分别加水稀释1000倍,其pH值与所加水的体积变化如图所示;则下列结论正确的是( )
常温下,等体积pH值等于2的两种酸溶液HA和HB,分别加水稀释1000倍,其pH值与所加水的体积变化如图所示;则下列结论正确的是( )| A、HB是弱酸,HA是强酸 |
| B、酸HA是比酸HB更强的酸 |
| C、稀释前酸HA的物质的量浓度大 |
| D、酸HB是比酸HA更强的酸 |
 有一透明溶液,可能含有较多的NH4+、Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32- 中的一种或几种,取此溶液做下列实验:
有一透明溶液,可能含有较多的NH4+、Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32- 中的一种或几种,取此溶液做下列实验: 如图表示A--E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色,写出各步反应的化学方程式.
如图表示A--E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色,写出各步反应的化学方程式.