题目内容
14.设NA为阿伏加德罗常数,下列说法正确的是( )| A. | 60g二氧化硅晶体中含有2NA个硅氧键 | |
| B. | 1molD2O中含有10NA个质子 | |
| C. | 12g金刚石中含有NA个碳碳键 | |
| D. | 1mol石墨晶体中含有2NA个碳碳键 |
分析 A、求出二氧化硅的物质的量,然后根据1mol二氧化硅中含4mol硅氧键来分析;
B、重水中含10个质子;
C、求出金刚石的物质的量,然后根据1mol金刚石中含2mol碳碳键来分析;
D、一个碳原子含有$\frac{3}{2}$个共价键,根据碳原子的个数计算共价键个数.
解答 解:A、60g二氧化硅的物质的量为n=$\frac{60g}{60g/mol}$=1mol,而1mol二氧化硅中含4mol硅氧键,故含4NA个,故A错误;
B、重水中含10个质子,故1mol重水中含10mol质子即10NA个,故B正确;
C、12g金刚石的物质的量为1mol,而1mol金刚石中含2mol碳碳键,故含2NA个,故C错误;
D、一个碳原子含有$\frac{3}{2}$个共价键,所以1mol石墨晶体中含有共价键键数为$\frac{3}{2}$NA,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.有四种短周期元素(除稀有气体之外)X、Y、M、N,其中X是短周期中金属性最强的元素;Y原子的最外层电子数是最内层电子数的3倍,是电子层数的2倍;M的单质是一种有色气体,可用于自来水的消毒;N的最高价氧化物对应的水化物是药物胃舒平的有效成分,该药物用于治疗胃酸过多.下列说法正确的是( )
| A. | X有两种常见氧化物,所含的化学键类型完全相同 | |
| B. | N与M形成的化合物的水溶液显酸性 | |
| C. | 离子半径:N>X,Y>M | |
| D. | 气态氢化物的稳定性:Y>M |
9.已知C-C键可以绕键轴自由旋转,结构简式为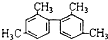 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )
 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )| A. | 分子中至少有9个碳原子处于同一平面上 | |
| B. | 分子中至少有11个碳原子处于同一平面上 | |
| C. | 该有机物不能使酸性KMnO4溶液褪色 | |
| D. | 该烃属于苯的同系物 |
19.下列物质以任意比混合,只要混合物的质量不变,完全燃烧后产生CO2的质量也不变的是( )
| A. | 乙醛和乙酸乙酯 | B. | 甲酸和乙酸 | ||
| C. | 甲醛和乙醇 | D. | 甲酸甲酯和乙酸乙酯 |
6.在100℃时,将甲醇.甲烷.氧气的混合气体放入一装有过量Na2O2固体的密闭容器中,不断用电火花引燃,充分反应后,测得密闭容器内气体压强为零,则原混合气体中甲醇.甲烷.氧气的体积比可能是( )
| A. | 1:1:1 | B. | 1:2:1 | C. | 1:3:2 | D. | 无法计算 |
3.下列名词中,不属于物理量的是( )
| A. | 长度 | B. | 时间 | C. | 物质的量 | D. | 摩尔 |
4.下列对有关化学反应过程或实验现象的解释正确的是( )
| A. | Cl2的水溶液可以导电,说明Cl2是电解质 | |
| B. | 某溶液中加入硝酸酸化的氯化钡溶液有白色沉淀生成说明溶液中一定含有SO42- | |
| C. | 向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2 | |
| D. | 切开金属钠暴露在空气中,光亮表面逐渐变暗2Na+O2=Na2O2 |