题目内容
19.下列物质以任意比混合,只要混合物的质量不变,完全燃烧后产生CO2的质量也不变的是( )| A. | 乙醛和乙酸乙酯 | B. | 甲酸和乙酸 | ||
| C. | 甲醛和乙醇 | D. | 甲酸甲酯和乙酸乙酯 |
分析 无论以何种比例混合,只要混合物的总质量一定,完全燃烧生成CO2的质量也一定,则说明混合物各组分的分子中含碳量相等,据此对各选项进行判断.
解答 解:无论以何种比例混合,只要混合物的总质量一定,完全燃烧生成CO2的质量也一定,则说明混合物各组分的分子中含碳量相等,
A.乙醛的分子式为C2H4O,乙酸乙酯的分子式为:C4H8O2,二者的最简式相同,则含碳量相同,符合题意,故A正确;
B.甲酸的分子式为CH2O2,乙酸的分子式为C2H4O2,最简式为CH2O,二者的含碳量不同,不符合题意,故B错误;
C.甲醛的分子式为HCHO,乙醇的分子式为C2H6O,二者的含碳量相等,不符合题意,故C正确;
D.甲酸甲酯的分子式为C2H4O2,最简式为CH2O,乙酸乙酯的分子式为C4H8O2,最简式为C2H4O,二者的含碳量不相等,不符合题意,故D错误;
故选A.
点评 本题考查混合物反应的计算,题目难度中等,根据题干信息明确有机物分子中的含碳量相同为解答关键,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.体积为V mL、密度为ρ g•cm-3的溶液,含有相对分子质量为M的溶质m g,其物质的量浓度为c mol•L-1,溶质的质量分数为W%,下列表示式中不正确的是( )
| A. | c=$\frac{W1000ρ}{M}$ | B. | m=$\frac{VρW}{100}$ | C. | W%=$\frac{CM}{1000ρ}$% | D. | c=$\frac{1000m}{VM}$ |
10.下列分子中含有两个π键的组合是( )
①H2O ②CO2 ③H-C≡N ④NH3 ⑤N2 ⑥CH4.
①H2O ②CO2 ③H-C≡N ④NH3 ⑤N2 ⑥CH4.
| A. | ①③⑥ | B. | ②③⑤ | C. | ①②③⑥ | D. | ③④⑤⑥ |
14.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 60g二氧化硅晶体中含有2NA个硅氧键 | |
| B. | 1molD2O中含有10NA个质子 | |
| C. | 12g金刚石中含有NA个碳碳键 | |
| D. | 1mol石墨晶体中含有2NA个碳碳键 |
4.某高分子化合物的部分结构如图:关于该物质的下列说法中,正确的是( )
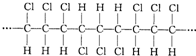

| A. | 合成该聚合物的单体是CHC1=CHC1 | |
| B. | 聚合物的链节(重复的基本结构单元)为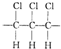 | |
| C. | 聚合物的分子式为C3H3C13 | |
| D. | 该聚合物可表示为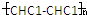 ,其中n为定值 ,其中n为定值 |
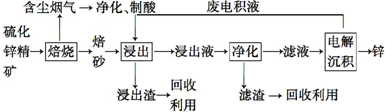
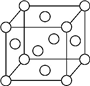 A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题: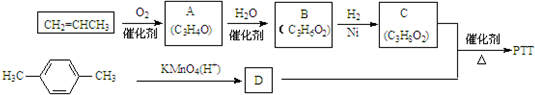
 .①分子式为C4H6O ②含有1个-CH3
.①分子式为C4H6O ②含有1个-CH3 ,反应类型为缩聚反应.
,反应类型为缩聚反应.