��Ŀ����
����������SnSO4����һ����Ҫ�������Σ���Ҫ���ڵ�ƹ�ҵ�Ķ��������Ͻ�����������ɫ��ӡȾ��ҵ��ýȾ����˫��ˮȥ�����ȣ�ij�о�С�����SnSO4�Ʊ�·�����£�

�������ϣ������������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ���������SnCl2��ˮ������������Sn��OH��Cl����ʽ�Ȼ�����������ش��������⣺
��1��SnCl2��ĩ���Ũ��������ܽ⣬����ƽ���ƶ�ԭ������ԭ�� ��
��2������Sn�۵��������������ٵ�����ҺpH�� ��
��3����Ӧ�����ɵ�����ΪCO2���õ��ij�����SnO���ó��������˺���Ưϴ�����֤�������Ѿ�ϴ����ȫ�� ��
��4���ಽ���������ľ���ʵ�鲽������ƿ����ǣ� ��
��5�����������£�SnSO4����������˫��ˮȥ������������Ӧ�����ӷ���ʽ�� ��
��6����С��ͨ�����з���������������Ʒ�Ĵ��ȣ����ʲ����뷴Ӧ�����ٽ��������������У������ķ�ӦΪ��Sn+2HCl��SnCl2+H2���ڼ��������FeCl3������֪Ũ�ȵ�K2Cr2O7�ζ����ɵ�Fe2+�������ķ�ӦΪ��6FeCl2+K2Cr2O7+14HCl��6FeCl3+2KCl+2CrCl3+7H2Oȡ1.226g ������Ʒ��������������Ӧ����ȥ0.1000mol/L K2Cr2O7��Һ32.00mL�����������Ʒ���������������� ��

�������ϣ������������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ���������SnCl2��ˮ������������Sn��OH��Cl����ʽ�Ȼ�����������ش��������⣺
��1��SnCl2��ĩ���Ũ��������ܽ⣬����ƽ���ƶ�ԭ������ԭ��
��2������Sn�۵��������������ٵ�����ҺpH��
��3����Ӧ�����ɵ�����ΪCO2���õ��ij�����SnO���ó��������˺���Ưϴ�����֤�������Ѿ�ϴ����ȫ��
��4���ಽ���������ľ���ʵ�鲽������ƿ����ǣ�
��5�����������£�SnSO4����������˫��ˮȥ������������Ӧ�����ӷ���ʽ��
��6����С��ͨ�����з���������������Ʒ�Ĵ��ȣ����ʲ����뷴Ӧ�����ٽ��������������У������ķ�ӦΪ��Sn+2HCl��SnCl2+H2���ڼ��������FeCl3������֪Ũ�ȵ�K2Cr2O7�ζ����ɵ�Fe2+�������ķ�ӦΪ��6FeCl2+K2Cr2O7+14HCl��6FeCl3+2KCl+2CrCl3+7H2Oȡ1.226g ������Ʒ��������������Ӧ����ȥ0.1000mol/L K2Cr2O7��Һ32.00mL�����������Ʒ����������������
���㣺�Ʊ�ʵ�鷽�������,���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��,̽�����ʵ���ɻ�������ʵĺ���
ר�⣺ʵ�������
������SnCl2��ĩ��Ũ��������ܽ�õ�������Һ����ʱ��Һ�к���Sn2+��Sn4+�������м���Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpHֵ������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+�����˵�SnCl2��Һ�������м�̼���ƣ���SnԪ����SnO��ʽ����������ϴ�ӵô�����SnO����ϡ���ᣬ��SnSO4��Һ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ��Ƶ�SnSO4���壻
��1��SnCl2��ˮ�з���ˮ�ⷴӦ������HCl����ʹˮ��ƽ�����淴Ӧ�����ƶ�������Sn2+ˮ�⣻
��2�����������������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ�����������Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpH������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+��
��3�����˺�������ϴ��ԭ����
��4������Һ�õ�����ķ���������Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
��5�����������£�SnSO4����������˫��ˮȥ��������SnSO4�����������º�˫��ˮ��Ӧ��Sn2+�л�ԭ�ԣ�˫��ˮ�������ԣ�����Ӧ���ǣ�Sn4+��H2O������ʽΪ��Sn2++H2O2+2H+��Sn4++2H2O��
��6���٢ڢ۷����ķ�Ӧ�ֱ�ΪSn+2HCl��SnCl2+H2���٣�SnCl2+2FeCl3=SnCl4+2FeCl2�ڣ�6FeCl2+K2Cr2O7+14HCl��6FeCl3+2KCl+2CrCl3+7H2O6Sn��K2Cr2O7���ɷ���ʽ�٢ڢ۵�֪K2Cr2O7��6FeCl2��3SnCl2��3Sn��
n��Sn��=3n��K2Cr2O7��=3��0.1000mol/L��0.032L=0.0096mol��m��Sn��=n��Sn����M��Sn��=0.0096mol��119g/mol=1.1424g
������Ʒ��������������=
��100%=
��100%=93.18%��
��1��SnCl2��ˮ�з���ˮ�ⷴӦ������HCl����ʹˮ��ƽ�����淴Ӧ�����ƶ�������Sn2+ˮ�⣻
��2�����������������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ�����������Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpH������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+��
��3�����˺�������ϴ��ԭ����
��4������Һ�õ�����ķ���������Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
��5�����������£�SnSO4����������˫��ˮȥ��������SnSO4�����������º�˫��ˮ��Ӧ��Sn2+�л�ԭ�ԣ�˫��ˮ�������ԣ�����Ӧ���ǣ�Sn4+��H2O������ʽΪ��Sn2++H2O2+2H+��Sn4++2H2O��
��6���٢ڢ۷����ķ�Ӧ�ֱ�ΪSn+2HCl��SnCl2+H2���٣�SnCl2+2FeCl3=SnCl4+2FeCl2�ڣ�6FeCl2+K2Cr2O7+14HCl��6FeCl3+2KCl+2CrCl3+7H2O6Sn��K2Cr2O7���ɷ���ʽ�٢ڢ۵�֪K2Cr2O7��6FeCl2��3SnCl2��3Sn��
n��Sn��=3n��K2Cr2O7��=3��0.1000mol/L��0.032L=0.0096mol��m��Sn��=n��Sn����M��Sn��=0.0096mol��119g/mol=1.1424g
������Ʒ��������������=
| m(Sn) |
| m(��Ʒ) |
| 1.1424g |
| 1.226g |
���
�⣺SnCl2��ĩ��Ũ��������ܽ�õ�������Һ����ʱ��Һ�к���Sn2+��Sn4+�������м���Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpHֵ������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+�����˵�SnCl2��Һ�������м�̼���ƣ���SnԪ����SnO��ʽ����������ϴ�ӵô�����SnO����ϡ���ᣬ��SnSO4��Һ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ��Ƶ�SnSO4���壻
��1��SnCl2��ˮ�з���ˮ�ⷴӦ��SnCl2+H2O�TSn��OH��Cl+HCl�����淴Ӧ��Ӧ���ÿ���ţ�������������Sn��OH��Cl����Һ�������ʣ�������HCl����ʹƽ�����淴Ӧ�����ƶ�������Sn2+ˮ�⣻
�ʴ�Ϊ���������ᣬʹˮ��ƽ�������ƶ�������Sn2+ˮ�⣻
��2�����������������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ�����������Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpH������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+��
�ʴ�Ϊ����ֹSn2+��������
��3����Ӧ��Ϊ��SnCl2��Һ�м�̼���ƣ��õ��ij���ΪSnO���ó��������˺��渽����Cl-��Ҫ����������Ƿ�ϴ�Ӹɾ���ֻҪ�������һ��ϴ��Һ���Ƿ���Cl-����û�У���֤���Ѿ�ϴ�Ӹɾ�������û��ϴ�Ӹɾ�����AgNO3��Һ����Cl-��������ȡ���һ��ϴ��Һ�������м���AgNO3��Һ������������˵����ϴ�Ӹɾ���
�ʴ�Ϊ��ȡ���һ��ϴ��Һ�������м���AgNO3��Һ������������˵����ϴ�Ӹɾ���
��4����Ӧ���Ѿ��õ�SnSO4��Һ������Һ�õ�����ķ���������Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
�ʴ�Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
��5�����������£�SnSO4����������˫��ˮȥ��������SnSO4�����������º�˫��ˮ��Ӧ��Sn2+�л�ԭ�ԣ�˫��ˮ�������ԣ�����Ӧ���ǣ�Sn4+��H2O������ʽΪ��Sn2++H2O2+2H+=Sn4++2H2O��
�ʴ�Ϊ��Sn2++H2O2+2H+=Sn4++2H2O��
��6���٢ڢ۷����ķ�Ӧ�ֱ�ΪSn+2HCl��SnCl2+H2���٣�SnCl2+2FeCl3=SnCl4+2FeCl2�ڣ�6FeCl2+K2Cr2O7+14HCl��6FeCl3+2KCl+2CrCl3+7H2O6Sn��K2Cr2O7���ɷ���ʽ�٢ڢ۵�֪K2Cr2O7��6FeCl2��3SnCl2��3Sn��
n��Sn��=3n��K2Cr2O7��=3��0.1000mol/L��0.032L=0.0096mol��m��Sn��=n��Sn����M��Sn��=0.0096mol��119g/mol=1.1424g��
������Ʒ��������������=
��100%=
��100%=93.18%��
�ʴ�Ϊ��93.18%��
��1��SnCl2��ˮ�з���ˮ�ⷴӦ��SnCl2+H2O�TSn��OH��Cl+HCl�����淴Ӧ��Ӧ���ÿ���ţ�������������Sn��OH��Cl����Һ�������ʣ�������HCl����ʹƽ�����淴Ӧ�����ƶ�������Sn2+ˮ�⣻
�ʴ�Ϊ���������ᣬʹˮ��ƽ�������ƶ�������Sn2+ˮ�⣻
��2�����������������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ�����������Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpH������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+��
�ʴ�Ϊ����ֹSn2+��������
��3����Ӧ��Ϊ��SnCl2��Һ�м�̼���ƣ��õ��ij���ΪSnO���ó��������˺��渽����Cl-��Ҫ����������Ƿ�ϴ�Ӹɾ���ֻҪ�������һ��ϴ��Һ���Ƿ���Cl-����û�У���֤���Ѿ�ϴ�Ӹɾ�������û��ϴ�Ӹɾ�����AgNO3��Һ����Cl-��������ȡ���һ��ϴ��Һ�������м���AgNO3��Һ������������˵����ϴ�Ӹɾ���
�ʴ�Ϊ��ȡ���һ��ϴ��Һ�������м���AgNO3��Һ������������˵����ϴ�Ӹɾ���
��4����Ӧ���Ѿ��õ�SnSO4��Һ������Һ�õ�����ķ���������Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
�ʴ�Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
��5�����������£�SnSO4����������˫��ˮȥ��������SnSO4�����������º�˫��ˮ��Ӧ��Sn2+�л�ԭ�ԣ�˫��ˮ�������ԣ�����Ӧ���ǣ�Sn4+��H2O������ʽΪ��Sn2++H2O2+2H+=Sn4++2H2O��
�ʴ�Ϊ��Sn2++H2O2+2H+=Sn4++2H2O��
��6���٢ڢ۷����ķ�Ӧ�ֱ�ΪSn+2HCl��SnCl2+H2���٣�SnCl2+2FeCl3=SnCl4+2FeCl2�ڣ�6FeCl2+K2Cr2O7+14HCl��6FeCl3+2KCl+2CrCl3+7H2O6Sn��K2Cr2O7���ɷ���ʽ�٢ڢ۵�֪K2Cr2O7��6FeCl2��3SnCl2��3Sn��
n��Sn��=3n��K2Cr2O7��=3��0.1000mol/L��0.032L=0.0096mol��m��Sn��=n��Sn����M��Sn��=0.0096mol��119g/mol=1.1424g��
������Ʒ��������������=
| m(Sn) |
| m(��Ʒ) |
| 1.1424g |
| 1.226g |
�ʴ�Ϊ��93.18%��
������������Ҫ�������ʵķ����ᴿ��������Ϣ������Ӧ�á��������ʵĺ������õ��ಽ��Ӧ�ó��������Ĺ�ϵ��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
���ݻ�һ�����ܱ������У���ӦA��g��+2B��g��?2C��g����ƽ�⣬���ʼA��B�����ʵ����ֱ�ΪXmol��Ymol����Ҫʹƽ��ʱ��Ӧ�������ʵ����������������ʵ�����ȣ���
Ӧ������ǣ�������
| X |
| Y |
A��1��
| ||
B��3��
| ||
C��0.25��
| ||
D��0.25��
|
ͬ���칹���������л���ѧ���Ƿdz��ձ�ģ������л��ﻥΪͬ���칹����Ǣ� ��
�� ��
�� ��HC��CCH3 ��CH3CH2CH3 ��CH3CH=CHCH3��������
��HC��CCH3 ��CH3CH2CH3 ��CH3CH=CHCH3��������
 ��
�� ��
�� ��HC��CCH3 ��CH3CH2CH3 ��CH3CH=CHCH3��������
��HC��CCH3 ��CH3CH2CH3 ��CH3CH=CHCH3��������| A���ٺ͢� | B���ٺ͢� |
| C���ٺ͢� | D���ۺ͢� |
�й���ͼװ�õ�˵������ȷ���ǣ�������


| A���������뻹ԭ������ֱ�ӽӴ������ܷ�����Ӧ |
| B���ҳ��е缫��ӦʽΪNO3-+4H++e-�TNO2��+2H2O |
| C����ͭ����������6.4gʱ���׳���Һ��������6.4g |
| D����ͭ����������6.4gʱ�����ҳ��ܷ����ͨ���״����1.12L O2����ʹ����ȫ������ˮ |

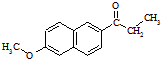 ���⣬��������ɵĸ������G��Ϊͬ���칹�壩�Ľṹ��ʽΪ
���⣬��������ɵĸ������G��Ϊͬ���칹�壩�Ľṹ��ʽΪ ����������X��C��ͬ���칹�壬�����к���2��ȡ��������ȡ������ͬһ�������ϣ�X��NaOH��Һ����ȫˮ���������ˮ�����ĺ˴Ź���������5���壮д��X���ܵĽṹ��ʽ��
����������X��C��ͬ���칹�壬�����к���2��ȡ��������ȡ������ͬһ�������ϣ�X��NaOH��Һ����ȫˮ���������ˮ�����ĺ˴Ź���������5���壮д��X���ܵĽṹ��ʽ�� �ĺϳ�·������ͼ�����Լ����ã���
�ĺϳ�·������ͼ�����Լ����ã���



