题目内容
7.下列酸溶液在相同温度下配制,其中pH值最小的是( )| A. | 0.1mol/L盐酸 | B. | 0.01mol/L盐酸 | C. | 0.1mol/L醋酸 | D. | 0.01mol/L醋酸 |
分析 溶液中氢离子浓度越大,溶液的酸性越强,该溶液的pH越小;弱电解质部分电离,强电解质完全电离,据此对各选项进行判断.
解答 解:A.0.1mol/L盐酸中氢离子浓度为0.1mol/L;
B.0.01mol/L的盐酸中氢离子浓度为0.01mol/L;
C.0.1mol/L的醋酸中氢离子浓度小于0.1mol/L;
D.0.01mol/L的醋酸溶液中氢离子浓度小于0.01mol/L;
根据分析可知,氢离子浓度增大的为0.1mol/L的盐酸,该溶液的pH最小,
故选A.
点评 本题考查了溶液酸碱性与溶液pH的关系,题目难度不大,明确氢离子浓度与溶液pH的关系为解答关键,注意掌握弱电解质的电离特点,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
15.在有机合成中,下列反应类型一定不能使有机物碳链增长的是( )
| A. | 取代反应 | B. | 加成反应 | C. | 聚合反应 | D. | 消去反应 |
2.某种有机物的结构简式为:
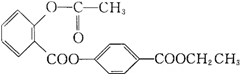
当它完全水解时,可得到的产物有( )

当它完全水解时,可得到的产物有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
3.某化学课外兴趣小组用实验的方法进行影响化学反应速率的因素.
(1)实验一:已知:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑
△H<0,酸性KMnO4溶液和H2C2O4溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快.
①某同学认为酸性KMnO4与H2C2O4溶液反应时反应速率明显加快,是因为反应放热使溶液温度升高.从影响化学反应速率的因素看,你的猜想还可能是催化剂(或锰离子的催化作用)的影响.
②若用实验证明你的猜想,除需要酸性KMnO4溶液、H2C2O4溶液外,还需要选择的试剂最合理的是b(填字母序号).
a.K2SO4 b.MnSO4 c.H2O d.MnO2
(2)实验二:探究酸的浓度对MnO2与H2O2反应速率的影响.
已知:MnO2+H2O2+2H+═Mn2++2H2O+O2↑,现取等量的MnO2和下表中的有关物质在相同温度下进行4组实验,分别记录收集等体积氧气所需的时间.
①上表中v1=5.0,v2=5.0.
②有同学提出实验Ⅰ不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是实验Ⅰ中MnO2作催化剂,其他三组实验中二氧化锰作氧化剂,反应原理不同.
③若实验测得t2>t3>t4,则可得出的实验结论是酸浓度越大,反应速率越快.
(1)实验一:已知:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑
△H<0,酸性KMnO4溶液和H2C2O4溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快.
①某同学认为酸性KMnO4与H2C2O4溶液反应时反应速率明显加快,是因为反应放热使溶液温度升高.从影响化学反应速率的因素看,你的猜想还可能是催化剂(或锰离子的催化作用)的影响.
②若用实验证明你的猜想,除需要酸性KMnO4溶液、H2C2O4溶液外,还需要选择的试剂最合理的是b(填字母序号).
a.K2SO4 b.MnSO4 c.H2O d.MnO2
(2)实验二:探究酸的浓度对MnO2与H2O2反应速率的影响.
已知:MnO2+H2O2+2H+═Mn2++2H2O+O2↑,现取等量的MnO2和下表中的有关物质在相同温度下进行4组实验,分别记录收集等体积氧气所需的时间.
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | v1 | v2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | v3 |
| 水的体积/mL | 15 | 14.5 | v4 | 13.5 |
| 所需时间/min | t1 | t2 | t3 | t4 |
②有同学提出实验Ⅰ不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是实验Ⅰ中MnO2作催化剂,其他三组实验中二氧化锰作氧化剂,反应原理不同.
③若实验测得t2>t3>t4,则可得出的实验结论是酸浓度越大,反应速率越快.
1.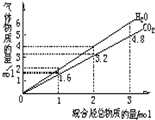 两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量变化如图所示,则下列对混合烃的判断正确的是( )
 两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量变化如图所示,则下列对混合烃的判断正确的是( )| A. | 一定含有甲烷 | B. | 一定含有乙烯 | C. | 一定含有丙炔 | D. | 一定不含乙烯 |
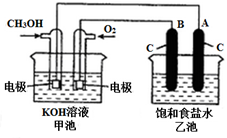 甲醇是一种可再生能源,具有广泛的开发和应用前景.如图是用甲醇燃料电池电解饱和食盐水的装置示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O
甲醇是一种可再生能源,具有广泛的开发和应用前景.如图是用甲醇燃料电池电解饱和食盐水的装置示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O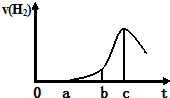 某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图.
某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图. 甲烷可用氧化铁作催化剂实现选择性地催化脱硝.
甲烷可用氧化铁作催化剂实现选择性地催化脱硝.