题目内容
12. 甲烷可用氧化铁作催化剂实现选择性地催化脱硝.
甲烷可用氧化铁作催化剂实现选择性地催化脱硝.氧化铁催化机理如图所示,有关热化学方程式如下:
N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1
(1)脱硝机理中第Ⅱ步的化学方程式为4Fe3O4+2NO=6Fe2O3+N2.
(2)CH4脱硝(N0)生成N2和液态水的热化学方程式为2CH4(g)+2NO(g)+3O2(g)═2CO2(g)+4H2O(l)+N2(g),△H=-1960kJ•mol-1;.
分析 (1)依据氧化铁催化机理图可知脱硝机理中第Ⅱ步四氧化三铁与一氧化氮反应生成氧化三铁和氮气;
(2)①N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1
②CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1;
②×2-①得:2CH4(g)+2NO(g)+3O2(g)═2CO2(g)+4H2O(l)+N2(g),依据盖斯定律计算反应热;
解答 解:(1)依据氧化铁催化机理图可知脱硝机理中第Ⅱ步四氧化三铁与一氧化氮反应生成氧化三铁和氮气,方程式:4Fe3O4+2NO=6Fe2O3+N2,
故答案为:4Fe3O4+2NO=6Fe2O3+N2;
(2)①N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1
②CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1;
②×2-①得:2CH4(g)+2NO(g)+3O2(g)═2CO2(g)+4H2O(l)+N2(g),△H,依据盖斯定律△H=2△H2-△H1=-890kJ•mol-1×2-180kJ•mol-1
=-1960kJ•mol-1;
所以反应的热化学方程式:2CH4(g)+2NO(g)+3O2(g)═2CO2(g)+4H2O(l)+N2(g),△H=-1960kJ•mol-1;
故答案为:2CH4(g)+2NO(g)+3O2(g)═2CO2(g)+4H2O(l)+N2(g),△H=-1960kJ•mol-1;
点评 本题考查了氧化还原方程式、热化学方程式书写,明确反应机理,熟悉盖斯定律计算反应热的方法即可解答,题目难度不大.

练习册系列答案
相关题目
3.下列说法不正确的是( )
| A. | Penguinone分子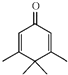 所有碳原子不可能都在同一个平面上 所有碳原子不可能都在同一个平面上 | |
| B. | 1mol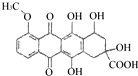 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol | |
| C. | 醋酸和软脂酸互为同系物,C5H12和C9H20也一定互为同系物 | |
| D. | 蛋白质遇到醋酸铅生成沉淀,加入大量的水,沉淀还可溶解 |
20.下列各项中,表达正确的是( )
| A. | O原子的结构示意图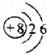 | B. | CH4分子的比例模型 | ||
| C. | C2H2分子的结构式CH≡CH | D. | N2分子的电子式 |
7.下列酸溶液在相同温度下配制,其中pH值最小的是( )
| A. | 0.1mol/L盐酸 | B. | 0.01mol/L盐酸 | C. | 0.1mol/L醋酸 | D. | 0.01mol/L醋酸 |
8.生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应).
相关资料
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在.
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计.
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化.
实验过程
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(l)请完成以下实验设计表(表中不要留空格)
实验测得含氰废水中的总氰浓度(以CN-表示)随时间变化关系如图所示.
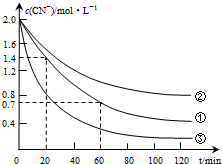
(2)实验①中20~60min时间段反应速率:υ(CN-)=0.0175mol•L-1•min-1.
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用(或初始pH增大,[Fe(CN)6]3-较中性和酸性条件下更稳定,难以氧化(填一点即可).在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO3-,同时放出NH3,试写出该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成下表中内容.(己知:废水中的CN-浓度可用离子色谱仪测定)
相关资料
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在.
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计.
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化.
实验过程
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(l)请完成以下实验设计表(表中不要留空格)
| 实验 序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
| ① | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
| ② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| ③ | 双氧水的浓度对破氰反应速率的影响 | 7 | 60 | 10 | 20 | 10 |

(2)实验①中20~60min时间段反应速率:υ(CN-)=0.0175mol•L-1•min-1.
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用(或初始pH增大,[Fe(CN)6]3-较中性和酸性条件下更稳定,难以氧化(填一点即可).在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO3-,同时放出NH3,试写出该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成下表中内容.(己知:废水中的CN-浓度可用离子色谱仪测定)
| 实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |
6.下列反应的离子方程式正确的是( )
| A. | NaAlO2溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+CO32- | |
| B. | NO2溶于水:3NO2+H2O=2H+$_{\;}^+$+2NO3-+NO | |
| C. | 醋酸溶液与水垢中的Mg(OH)2反应:Mg(OH)2+2H+═Mg2++2H2O | |
| D. | NaClO溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3- |
 .有机物X的键线式为
.有机物X的键线式为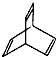
 .
.