题目内容
14.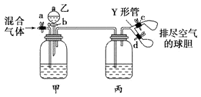 用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )
用如图装置来分离CO2和CO混合气体,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为( )| 甲 | 乙 | 丙 | |
| A | 饱和NaHCO3溶液 | 12mol•L-1盐酸 | 18.4mol•L-1 H2SO4 |
| B | 饱和Na2CO3溶液 | 2mol•L-1 H2SO4 | 饱和NaOH溶液 |
| C | 饱和NaOH溶液 | 2mol•L-1 H2SO4 | 18.4mol•L-1 H2SO4 |
| D | 18.4mol•L-1 H2SO4 | 饱和NaOH溶液 | 18.4mol•L-1 H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
分析 用图中装置来分离CO2和CO混合气体,甲中为NaOH溶液,混合气体进入甲中,只有CO不反应,则CO进入丙中干燥,最后收集在球胆中;乙中可为稀硫酸,打开b,与甲中溶液反应可生成二氧化碳,然后收集,以此来解答.
解答 解:由图可知,甲吸收二氧化碳,丙为干燥气体,乙为酸,则甲为饱和NaOH溶液,乙为2mol•L-1 H2SO4,丙为18.4mol•L-1 H2SO4,先关闭b,打开c或d收集CO,再关闭c或d,打开b,同时打开d或c,收集二氧化碳,
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的性质、发生的反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
相关题目
5.乙酸的下列性质中,可以证明它是弱电解质的是( )
| A. | 乙酸与水能以任意比例互溶 | |
| B. | 乙酸溶液的导电性弱 | |
| C. | 10 mL1 mol•L-1乙酸恰好与10 mL1 mol•L-1NaOH溶液完全反应 | |
| D. | 1 mol•L-1的乙酸溶液的C(H+)约为0.01 mol•L-1 |
5.反应N2(g)+O2(g)═2NO(g)的过程中的能量变化如图所示,下列有关说法中正确的是( )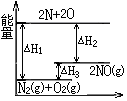

| A. | △H3>0 | B. | △H2为该反应的反应热 | ||
| C. | 反应N2(g)+O2(g)═2NO(g)为放热反应 | D. | △H3=△H1-△H2 |
2.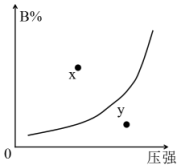 在一定温度下,反应mA(s)+nB(g)?pC(g)△H<0,B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
在一定温度下,反应mA(s)+nB(g)?pC(g)△H<0,B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
 在一定温度下,反应mA(s)+nB(g)?pC(g)△H<0,B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
在一定温度下,反应mA(s)+nB(g)?pC(g)△H<0,B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )| A. | m+n>P | |
| B. | x点表示该反应的正反应速率小于逆反应速率 | |
| C. | n<p | |
| D. | x点比y点时的反应速率快 |
9.用惰性电极电解下列溶液,电解一断时间后,阴极质量增加,电解液的pH下降的是( )
| A. | CuSO4 | B. | HCl | C. | BaCl2 | D. | Na2SO4 |
6.下列各物质投入水中,因促进水的电离而使溶液呈酸性的是( )
| A. | NaHSO4 | B. | Na3PO4 | C. | CH3COOH | D. | Al2(SO4)3 |
3.将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
| A. | 硫酸锌 | B. | 氯水 | C. | 氯化铜 | D. | 硝酸钠 |
4.下列叙述正确的是( )
| A. | 在蒸馏水中滴加稀H2SO4,c(H+)和KW都增大 | |
| B. | 等体积0.2mol/LHCl溶液与0.05mol/LBa(OH)2溶液混合后,溶液的pH=1 | |
| C. | NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| D. | 在Na2CO3溶液中,c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |