题目内容
8.从下列选项中选择适当的字母填入空格A、渗析 B、布朗运动 C、聚沉 D、丁达尔效应 E、电泳
(1)氢氧化铁胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近颜色加深,这种现象叫E
(2)强光通过氢氧化铁胶体,可看到光带,这种现象叫D
(3)淀粉和食盐混合液放在半透膜中,悬挂在盛有蒸馏水的烧杯里,从而使它们分离,这种方法叫A
(4)氢氧化铁胶体加入硅酸胶体,胶体变浑浊,这是发生了C.
分析 (1)依据胶粒吸附带电离子分析判断;
(2)依据胶体的性质分析判断;
(3)从溶液和胶体的分离分析判断;
(4)从胶体的性质聚沉分析判断.
解答 解:(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,说明胶粒吸附了正电荷,这种现象为电泳,故答案为:E;
(2)强光通过Fe(OH)3胶体,可看到光带,是粒子对光的散射作用形成的是胶体的性质,称为丁达尔现象,故答案为:D;
(3)淀粉与食盐的混合液放在肠衣中,并把它悬挂在盛有蒸馏水的烧瓶里,从而使淀粉与食盐分离,利用了胶体不能通过半透膜的性质,称为渗析,故答案为:A;
(4)Fe(OH)3胶体加硅酸胶体,胶体变得浑浊,是因为氢氧化铁胶体微粒吸附正电荷,硅酸胶体微粒吸附负电荷,二者混合会发生聚沉,是胶体的性质,故答案为:C.
点评 本题考查了胶体的性质应用,主要是电泳、丁达尔现象、渗析、聚沉等性质的判断,较简单.

练习册系列答案
相关题目
18.化学与生产、生活密切相关.下列说法正确的是( )
| A. | 福尔马林可用于保存海鲜产品 | |
| B. | 硅胶吸附能力强,常用作催化剂载体和食品干燥剂 | |
| C. | 工业上利用Cl2与澄清石灰水反应制取漂白粉 | |
| D. | 天然纤维和合成纤维的主要成分是纤维素 |
19.已知短周期元素的四种离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A. | 原子序数 d>c>b>a | |
| B. | 单质的还原性D<C<B<A | |
| C. | 离子半径 C3->D->B+>A2+ | |
| D. | A、B、C最高价氧化物对应水化物溶液(等物质的量浓度)的pH值C>B>A |
16.反应2SO2+O2$?_{△}^{催化剂}$2SO3经一段时间后,SO3的浓度增加了0.8mol•L-1,在这段时间内用O2表示的反应速率为0.04mol•L-1•s-1,则这段时间为( )
| A. | 0.1 s | B. | 2.5 s | C. | 5 s | D. | 10 s |

 ,
,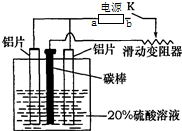 铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜.某化学研究小组在实验室中按下列步骤模拟该生产过程,装置如图.填写下列空白:
铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜.某化学研究小组在实验室中按下列步骤模拟该生产过程,装置如图.填写下列空白: