题目内容
20.下列对有关实验事实的说明或解释正确的是( )| A. | 浓硫酸和浓盐酸长期暴露在空气中浓度都会降低,但原理不相同 | |
| B. | 常温下,浓硫酸可以用铁制容器储存,说明铁与冷的浓硫酸不反应 | |
| C. | 向某溶液中加入盐酸酸化的氯化钡溶液,生成白色沉淀,说明原溶液中一定含有SO42- | |
| D. | 向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中一定含有Fe2+ |
分析 A.浓硫酸具有吸水性,浓度减小,浓盐酸是易挥发出氯化氢,溶液浓度减小;
B.浓硫酸和铁发生钝化反应;
C.可能生成AgCl沉淀;
D.加入试剂顺序错误,不能鉴别Fe2+.
解答 解:A.浓硫酸具有吸水性,浓度减小,浓盐酸是易挥发出氯化氢,溶液浓度减小,浓度减小的原理不同,故A正确;
B.浓硫酸和铁发生钝化反应,在表面生成一层致密的氧化物膜,阻碍反应的进一步进行,但不是不反应,故B错误;
C.可能生成AgCl沉淀,应先加入盐酸,如无现象,再加入氯化钡检验,故C错误;
D.加入试剂顺序错误,应先加入KSCN,在加入氯气,否则不能鉴别Fe2+,故D错误.
故选A.
点评 本题综合考查元素化合物知识,为高频考点,涉及离子的检验、以及元素化合物知识,注意把握物质的性质的异同以及实验的严密性和可行性的评价,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.实验是化学研究的基础,下列实验装置,试剂选用或惭怍正确的是( )
| A. |  除去CO2中的HCl | B. |  干燥Cl2 | C. |  稀释浓硫酸 | D. |  分离乙醇和水 |
15.下列有机化学反应方程式书写及反应类型均正确的是( )
| A. | CH3Cl+Cl2$\stackrel{光}{→}$CH2Cl2+HCl 取代反应 | |
| B. | H2C=CH2+Br2→CH3CHBr2 加聚反应 | |
| C. |  加成反应 加成反应 | |
| D. |  氧化反应 氧化反应 |
5.常温下,下列各组高于一定能在制定溶液中大量共存的是( )
| A. | pH=14的溶液中:NH4+、Al3+、Cl-、NO3- | |
| B. | 中性溶液中:Fe2+、K+、Cl-、${SO}_{4}^{2-}$ | |
| C. | 含有大量Ba2+的溶液中:Mg2+、Na+、${NO}_{3}^{-}$、Cl- | |
| D. | 由水电离出的c(H+)=1×10-12mol-1的溶液中:Na+、Mg2+、HCO3-、CH3COO- |
9.短周期主族元素Q、W、X、Y、Z的原子序数依次增大,它们互不同族,Q的一种同位素常用于文物年代鉴定,X、Y、Z的原子半径逐渐减小,w的单质是最稳定的双原子分子,X与Y质子数之和是W原子核外电子数的4倍.下列说法正确的是:( )
| A. | W的简单气态氰化物比Y的稳定 | |
| B. | XZ2与QY2中含有j的化学键类型相同 | |
| C. | 元素Q、Y的单质均只存在两种同素异形体 | |
| D. | Y的最高价氧化物对应水化物的酸性比Z的强 |
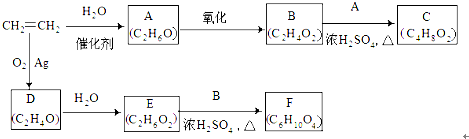
 E
E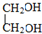 F
F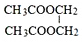 写出C酸性条件下水解的方程式CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$CH3COOH+CH3CH2OH
写出C酸性条件下水解的方程式CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$CH3COOH+CH3CH2OH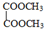 .
.
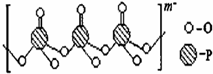 磷单质及其化合物在工业生产中有着广泛的应用.白磷可用于制备高纯度的磷酸(
磷单质及其化合物在工业生产中有着广泛的应用.白磷可用于制备高纯度的磷酸(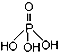 ),三聚磷酸钠(NaH2PO2)可用于化学镀镍等等.请回答下列问题:
),三聚磷酸钠(NaH2PO2)可用于化学镀镍等等.请回答下列问题: