题目内容
金属/空气燃料电池是一种正在逐步走向商品化的新型电池,非常适用于电动车等动力应用.
(1)和很多燃料电池一样,金属/空气燃料电池的还原剂为活泼金属,如锌、铝等;金属/空气燃料电池的氧化剂为空气中的 ,不需要储存在电池内.
(2)铝/空气燃料电池常使用3~5mol/L的NaOH溶液做电解质.该电池正极的电极反应为 ,负极的电极反应为 .
(3)铝是地壳中含量最多的金属元素.不过,直到电解法的出现,人类才开始大量使用金属铝.试计算,电解法冶炼金属铝时若有6mol电子发生转移,则在阴极上得到金属铝的质量是 g.
(1)和很多燃料电池一样,金属/空气燃料电池的还原剂为活泼金属,如锌、铝等;金属/空气燃料电池的氧化剂为空气中的
(2)铝/空气燃料电池常使用3~5mol/L的NaOH溶液做电解质.该电池正极的电极反应为
(3)铝是地壳中含量最多的金属元素.不过,直到电解法的出现,人类才开始大量使用金属铝.试计算,电解法冶炼金属铝时若有6mol电子发生转移,则在阴极上得到金属铝的质量是
考点:化学电源新型电池,电解原理
专题:电化学专题
分析:(1)燃料电池中,自发的氧化还原反应是燃料和氧气之间的反应,据此判断氧化剂;
(2)铝/空气燃料电池活泼的金属Al作负极,负极失电子发生氧化反应;正极为氧气得电子的还原反应,据此回答;
(3)根据电解氧化铝的方程式进行计算.
(2)铝/空气燃料电池活泼的金属Al作负极,负极失电子发生氧化反应;正极为氧气得电子的还原反应,据此回答;
(3)根据电解氧化铝的方程式进行计算.
解答:
解:(1)燃料电池中,自发的氧化还原反应是燃料和氧气之间的反应,金属/空气燃料电池的氧化剂为空气中的氧气,故答案为:O2;
(2)铝/空气燃料电池中,正极上是氧气得电子的还原反应:O2+2H2O+4e-=4OH-,负极上是金属铝失电子的氧化反应,在碱性环境下,电极反应式为:Al-3e-+4OH-=AlO2-+2H2O,故答案为:O2+2H2O+4e-=4OH-;Al-3e-+4OH-=AlO2-+2H2O;
(3)根据电解液炼铝的方程式:2Al2O3(熔融)
4Al+3O2↑,该反应生成金属铝4mol,会转移电子12moL,所以若有6mol电子发生转移,则在阴极上得到金属铝的物质的量是2mol,质量是54g,故答案为:54.
(2)铝/空气燃料电池中,正极上是氧气得电子的还原反应:O2+2H2O+4e-=4OH-,负极上是金属铝失电子的氧化反应,在碱性环境下,电极反应式为:Al-3e-+4OH-=AlO2-+2H2O,故答案为:O2+2H2O+4e-=4OH-;Al-3e-+4OH-=AlO2-+2H2O;
(3)根据电解液炼铝的方程式:2Al2O3(熔融)
| ||
点评:本题考查了原电池、电解池原理及电极反应式的书写,难度不大,注意电子守恒在电化学中的应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有A、B两份铝粉,A中加入足量NaOH溶液,B中加入足量盐酸,A、B两份铝粉反应收集到的氢气物质的量之比为1:2,则两份铝质量比为( )
| A、1:2 | B、2:1 |
| C、1:4 | D、1:1 |
漆酚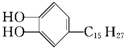 是生漆的主要成分,黄色,能溶于有机溶剂.生漆涂在物体表面能在空气中干燥而转变为黑色漆膜.下列关于漆酚说法错误的是( )
是生漆的主要成分,黄色,能溶于有机溶剂.生漆涂在物体表面能在空气中干燥而转变为黑色漆膜.下列关于漆酚说法错误的是( )
 是生漆的主要成分,黄色,能溶于有机溶剂.生漆涂在物体表面能在空气中干燥而转变为黑色漆膜.下列关于漆酚说法错误的是( )
是生漆的主要成分,黄色,能溶于有机溶剂.生漆涂在物体表面能在空气中干燥而转变为黑色漆膜.下列关于漆酚说法错误的是( )| A、可以燃烧,当氧气充分时,产物为CO2和H2O |
| B、与FeCl3溶液发生显色反应 |
| C、能发生取代反应和加成反应 |
| D、不能被酸性KMnO4溶液氧化 |