题目内容
写出下列元素的原子结构示意图、电子排布式、价电子排布式及周期表中的位置.
①9F 、 、 、 周期 族;
②25Mn 、 、 、 周期 族.
①9F
②25Mn
考点:原子结构示意图,元素周期表的结构及其应用,原子核外电子排布
专题:原子组成与结构专题,元素周期律与元素周期表专题
分析:9F为9号元素,原子核中有9个质子,核外9个电子,分别位于3个电子层上,最外层电子有7个,为价电子,根据电子层数和最外层电子数判断在周期表中的位置;
25Mn为25号元素,原子核中有25个质子,核外有25个电子,分别位于4个电子层,价电子有7个,其中有5个位于3d轨道上,2个位于4s轨道上,依据电子层数和价电子数判断在周期表中的位置.
25Mn为25号元素,原子核中有25个质子,核外有25个电子,分别位于4个电子层,价电子有7个,其中有5个位于3d轨道上,2个位于4s轨道上,依据电子层数和价电子数判断在周期表中的位置.
解答:
解:①9F为9号元素,原子核中有9个质子,核外9个电子,其原则结构示意图为: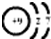 ;核外9个电子分别位于1s、2s、2p轨道,电子排布式为:1S22S22P5;最外层7个电子为价电子,价电子排布式为S22P5;依据电子层数等于周期数,最外层电子等于主族元素的族序数,9F位于第2周期VIIA族;
;核外9个电子分别位于1s、2s、2p轨道,电子排布式为:1S22S22P5;最外层7个电子为价电子,价电子排布式为S22P5;依据电子层数等于周期数,最外层电子等于主族元素的族序数,9F位于第2周期VIIA族;
②25Mn为25号元素,原子核中有25个质子,核外有25个电子,其原则结构示意图为: ;核外25个电子分别位于1s、2s、2p、3s、3p、3d、4s轨道,电子排布式为:[Ar]3d54S2,价电子有7个分别位于3d、4S两个轨道上,价电子排布式为3d54S2,周期序数等于电子层数,价电子数等于副族族序数,所以25Mn位于第4周期VIIB族;
;核外25个电子分别位于1s、2s、2p、3s、3p、3d、4s轨道,电子排布式为:[Ar]3d54S2,价电子有7个分别位于3d、4S两个轨道上,价电子排布式为3d54S2,周期序数等于电子层数,价电子数等于副族族序数,所以25Mn位于第4周期VIIB族;
故答案为:①9F;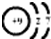 、1S22S22P5、2S22P5、第2周期VIIA族;
、1S22S22P5、2S22P5、第2周期VIIA族;
②25Mn; 、[Ar]3d54S2、3d54S2、第4周期VIIB族.
、[Ar]3d54S2、3d54S2、第4周期VIIB族.
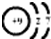 ;核外9个电子分别位于1s、2s、2p轨道,电子排布式为:1S22S22P5;最外层7个电子为价电子,价电子排布式为S22P5;依据电子层数等于周期数,最外层电子等于主族元素的族序数,9F位于第2周期VIIA族;
;核外9个电子分别位于1s、2s、2p轨道,电子排布式为:1S22S22P5;最外层7个电子为价电子,价电子排布式为S22P5;依据电子层数等于周期数,最外层电子等于主族元素的族序数,9F位于第2周期VIIA族;②25Mn为25号元素,原子核中有25个质子,核外有25个电子,其原则结构示意图为:
 ;核外25个电子分别位于1s、2s、2p、3s、3p、3d、4s轨道,电子排布式为:[Ar]3d54S2,价电子有7个分别位于3d、4S两个轨道上,价电子排布式为3d54S2,周期序数等于电子层数,价电子数等于副族族序数,所以25Mn位于第4周期VIIB族;
;核外25个电子分别位于1s、2s、2p、3s、3p、3d、4s轨道,电子排布式为:[Ar]3d54S2,价电子有7个分别位于3d、4S两个轨道上,价电子排布式为3d54S2,周期序数等于电子层数,价电子数等于副族族序数,所以25Mn位于第4周期VIIB族;故答案为:①9F;
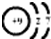 、1S22S22P5、2S22P5、第2周期VIIA族;
、1S22S22P5、2S22P5、第2周期VIIA族;②25Mn;
 、[Ar]3d54S2、3d54S2、第4周期VIIB族.
、[Ar]3d54S2、3d54S2、第4周期VIIB族.
点评:本题考查元素周期表、常用化学用语、核外电子排布规律等,题目难度不大,掌握元素周期表的结构和元素原子的结构式解题的关键.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
某固体混合物可能由Na2CO3、Na2SO4、CuSO4、KCl等混合而成,为检验其组成,依次进行下列实验,且每步所加试剂均过量,观察到的现象如表:
下列分析正确的是( )
| 步骤 | 操作 | 现象 |
| (1) | 将固体混合物溶于水,搅拌 | 溶液无色透明 |
| (2) | 向此溶液中滴加BaCl2溶液 | 出现白色沉淀 |
| (3) | 过滤,将沉淀物置于足量稀硝酸中 | 沉淀完全溶解,有气泡产生 |
| (4) | 向滤液中加入AgNO3和稀硝酸 | 有白色沉淀产生 |
| A、固体混合物中肯定有KCl |
| B、固体混合物中可能含有Na2SO4 |
| C、(2)中发生的离子反应为:Ba2++CO32-=BaCO3;Ba2++SO42-=BaSO4 |
| D、固体混合物中肯定含有Na2CO3 |
下列实验中没用温度计的是( )
| A、蒸馏石油实验 |
| B、酚醛树脂的制备 |
| C、乙醇在浓硫酸作用下发生消去反应 |
| D、硝基苯的制备 |
 某无色溶液中只含有下列离子中的某几种:Na+、Mg2+、SO42-、CO32-、Cl-、MnO4-.为了鉴别这些离子,分别取少量溶液进行以下实验:
某无色溶液中只含有下列离子中的某几种:Na+、Mg2+、SO42-、CO32-、Cl-、MnO4-.为了鉴别这些离子,分别取少量溶液进行以下实验: