题目内容
7.某氢氧固体酸燃料电池的总反应为:2H2+O2=2H2O,其基本结构如图所示: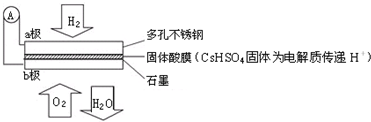
下列有关说法不正确的是( )
| A. | 电子通过外电路从a极流向b极 | |
| B. | H+由a极通过固体酸电解质传递到b极 | |
| C. | 电池工作时每转移0.1 mol电子,消耗1.12 LH2 | |
| D. | b极上的电极反应式为:O2+4H++4e-=2H2O |
分析 根据电池总反应:2H2+O2=2H2O可知:通入氢气的一极为电池的负极,发生氧化还原反应,反应为H2-2e-═2H+,通入氧气的一极为电池的正极,发生氧化反应,反应为O2+4e-+4H+=2H2O;电池工作时,电子通过外电路从负极流向正极,即从a极流向b极,电解质中阳离子向正极移动,即H+由a极通过固体酸电解质传递到b极;每转移0.1mol电子,消耗0.05mol的H2,生成0.05mol水,以此解答该题.
解答 解:根据电池总反应:2H2+O2=2H2O可知:通入氢气的一极为电池的负极,发生氧化还原反应,反应为H2-2e-═2H+,通入氧气的一极为电池的正极,发生氧化反应,反应为O2+4e-+4H+=2H2O;电池工作时,电子通过外电路从负极流向正极,即从a极流向b极,电解质中阳离子向正极移动,即H+由a极通过固体酸电解质传递到b极;每转移0.1mol电子,消耗0.05mol的H2,生成0.05mol水,
A.a为负极,b是正极,则电子应该是通过外电路由a极流向b,故A正确;
B.原电池中,阳离子向正极移动,所以H+由a极通过固体酸电解质传递到b极,故B正确;
C.每转移0.1mol电子,消耗0.05mol的H2,但气体存在的条件未知,体积不一定为1.12 L,故C错误;
D.该电池为酸性电池,所以正极电极反应为O2+4e-+4H+=2H2O,故D正确.
故选C.
点评 该题是高考中的常见题型,属于中等难度的试题.侧重考查学生灵活运用原电池原理解决实际问题的能力.学习中要明确原电池电子以及离子的定向移动问题,要能正确判断原电池的正负极,以及电极反应式的书写等问题.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
17.如图装置应用于实验室制备氯气并回收氯化锰的实验操作,能达到实验目的是( )
| A. |  用装置制取氯气 | |
| B. | 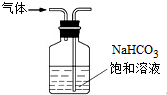 用装置除去氯气中混有的少量氯化氢 | |
| C. | 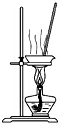 用装置蒸干氯化锰溶液制MnCl2•4H2O | |
| D. | 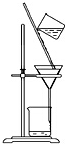 用装置分离二氧化锰和氯化锰溶液 |
18.已知在298K时,2g氢气与氧气完全反应生成液态水放热285.8kJ,则此反应的热化学方程式为( )
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ•mol-1 | |
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ•mol-1 |
15.下列仪器对应的名称正确的是( )
| A. | 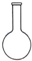 容量瓶 | B. |  萃取瓶 | C. | 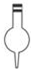 锥形瓶 | D. |  酸式滴定管 |
2.已知反应:C(s)+CO2(g)?2CO(g)△H>0一定条件下,改变某一个反应条件一定能使反应速率显著加快的是( )
| A. | 降低反应体系的压强 | B. | 增加反应物碳的用量 | ||
| C. | 缩小反应体系的体积 | D. | 减少体系中CO的量 |
19.某温度下,0.200mol•L-1的HA溶液与0.200mol•L-1的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下表,下列说法正确的是( )
| 微粒 | X | Y | Na+ | A- |
| 浓度/(mol•L-1) | 8.00×10-4 | 2.50×10-10 | 0.100 | 9.92×10-2 |
| A. | 0.1mol•L-1HA溶液的pH=1 | B. | 该温度下Kw=1.0×10-14 | ||
| C. | 微粒X表示OH-,Y表示H+ | D. | 混合溶液中:n(A-)+n(X)=n(Na+) |
16.在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)?H2(g)+I2(g),2s时生成0.1mol H2,则以HI表示该时段的化学反应速率是( )
| A. | 0.05 mol•Lˉ1•sˉ1 | B. | 0.1 mol•Lˉ1•sˉ1 | ||
| C. | 0.2 mol•Lˉ1•sˉ1 | D. | 0.8 mol•Lˉ1•sˉ1 |
14.将pH试纸用蒸馏水湿润后,去测定某盐酸的pH,测得的pH将比实际( )
| A. | 偏高 | B. | 偏低 | ||
| C. | 不变 | D. | 三种情况均有可能 |