题目内容
11.加热蒸发下列溶液,能析出得到原溶质的是( )| A. | KNO3溶液 | B. | FeCl3溶液 | C. | Al2(SO4)3溶液 | D. | FeSO4溶液 |
分析 溶液加热蒸干后,能析出原溶质固体的,需要溶质性质稳定,不分解、不能被氧化、不能水解或水解程度不大,据此分析.
解答 解:A、KNO3是强酸强碱盐,不能水解也不能分解,也不能被氧化,故加热蒸发能得到KNO3本身,故A正确;
B、FeCl3是强酸弱碱盐,在溶液中水解:FeCl3+3H2O?Fe(OH)3+3HCl,由于HCl是挥发性酸,故加热时挥发,导致水解被促进,则蒸干后得到的是Fe(OH)3,故B错误;
C、Al2(SO4)3是强酸弱碱盐,在溶液中会水解:Al2(SO4)3+6H2O?2Al(OH)3+3H2SO4,由于硫酸不挥发,故加热时水解被促进的程度很小,蒸干后Al(OH)3和H2SO4又能反应生成Al2(SO4)3,故得到的是溶质本身,故C正确;
D、FeSO4有强还原性,在蒸干时会被氧化为Fe2(SO4)3,得到的不是溶质本身,故D错误.
故选AC.
点评 本题考查盐类水解知识,题目难度不大,注意把握物质的稳定性和水解的性质,易错点为C,注意硫酸盐水解的特点.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
1.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+N2(g)△H<0
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2s内的平均反应速率υ(N2)=1.9×10-4mol/(L•s);CO的平衡转化率为25%.(结果均保留两位有效数字)
(2)写出该反应的平衡常数K的表达式$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$.
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是CD.
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.某同学设计了三组实验,实验条件已经填在下面实验设计表中.
①以上三组实验的实验目的是分别验证温度、催化剂比表面积对化学反应速率的影响规律.
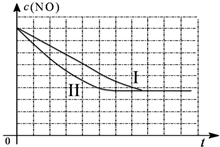
②请在给出的坐标图中,画出上表中的第三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图.
(5)已知CO的燃烧热为284kJ/mol,且N2(g)+O2(g)═2NO(g)△H=+180kJ/mol;则反应2NO(g)+2CO(g)?2CO2(g)+N2(g)△H=-748kJ/mol.
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO) (mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)前2s内的平均反应速率υ(N2)=1.9×10-4mol/(L•s);CO的平衡转化率为25%.(结果均保留两位有效数字)
(2)写出该反应的平衡常数K的表达式$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$.
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是CD.
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.某同学设计了三组实验,实验条件已经填在下面实验设计表中.
| 实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积 (m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
②请在给出的坐标图中,画出上表中的第三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图.

(5)已知CO的燃烧热为284kJ/mol,且N2(g)+O2(g)═2NO(g)△H=+180kJ/mol;则反应2NO(g)+2CO(g)?2CO2(g)+N2(g)△H=-748kJ/mol.
2.下列各组粒子所含电子数目相同的是( )
| A. | NH4+、OH-、H3O+ | B. | Na+、Mg2+、S2- | C. | F-、NH2-、Cl- | D. | Li+、Na+、K+ |
19.下列说法正确的是( )
| A. | 热的纯碱溶液去污能力强 | |
| B. | 硫酸钡、醋酸铵、氨水都是弱电解质 | |
| C. | 用Na2S溶液与AlCl3溶液混合制取Al2S3 | |
| D. | 碳酸钡和硫酸钡都可以用做钡餐 |
6.常温下,某溶液中由水电离的[H+]和[OH-]的乘积为1.0×10-22 mol2•L-2,则在该溶液中一定不能大量共存的离子组是( )
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | NH4+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
16.氯气是一种重要的工业原料,工业上利用反应3Cl2+2NH3═N2+6HCl检查氯气管道是否漏气,下列说法错误的是( )
| A. | 若管道漏气遇氨就会产生白烟 | B. | 该反应利用了Cl2的强氧化性 | ||
| C. | 该反应NH3被还原 | D. | 生成1 mol N2有6 mol电子转移 |
3.镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中的总反应方程式是:
Ni(OH)2+M═NiOOH+MH 已知:6NiOOH+NH3+H2O+OH-═6Ni(OH)2+NO2-
下列说法正确的是( )
Ni(OH)2+M═NiOOH+MH 已知:6NiOOH+NH3+H2O+OH-═6Ni(OH)2+NO2-
下列说法正确的是( )
| A. | 电池放电过程中,正极电极反应式为:NiOOH+H2O+e-═Ni(OH)2+OH- | |
| B. | 充电过程中阴极的电极反应式:H2O+M+e-═MH+OH-,H2O中的H被M还原 | |
| C. | 充电过程中OH-离子从阳极向阴极迁移 | |
| D. | NiMH电池中可以用KOH溶液、氨水等作为电解质溶液 |
1.某溶液中可能存在Fe3+、Fe2+、I-、HCO${\;}_{3}^{-}$、Cl-、NO${\;}_{3}^{-}$六种离子中的几种.进行下列实验:
①取少量溶液滴加KSCN溶液,溶液呈红色;
②另取少量原溶液滴加盐酸,溶液的棕黄色加深.
据此可以推断,该溶液中一定大量存在的阴离子是( )
①取少量溶液滴加KSCN溶液,溶液呈红色;
②另取少量原溶液滴加盐酸,溶液的棕黄色加深.
据此可以推断,该溶液中一定大量存在的阴离子是( )
| A. | I- | B. | HCO${\;}_{3}^{-}$ | C. | Cl- | D. | NO${\;}_{3}^{-}$ |