题目内容
2.常温下,某溶液 A 中含有 NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、Cl-、SO42-、SO32-,现取该溶液进行有关实验,实验结果如图所示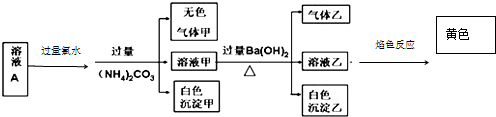
下列有关说法正确的是( )
| A. | 沉淀乙一定可溶于盐酸 | |
| B. | 溶液中一定存在 Na+、Al3+,一定没有 Fe3+、Fe2+、CO32- | |
| C. | 溶液中一定有 SO42-,可能有 K+、Cl- | |
| D. | 气体甲、乙均为无色、有刺激性气味 |
分析 根据流程可知:溶液A通入过量氯水、和过量的碳酸铵溶液后生成白色沉淀甲,该白色沉淀只能为氢氧化铝,氢氧化铁沉淀为红褐色,则原溶液最后一定不存在Fe2+、Fe3+,原溶液最后一定含有Al3+,根据离子共存可知一定不存在SO32-、CO32-;则生成的气体甲只能为二氧化碳气体;向溶液甲中通入氢氧化钡溶液后生成白色沉淀乙,由于碳酸铵过量,白色沉淀乙中一定含有BaCO3,可能含有BaSO4;气体乙为氨气,溶液乙的焰色反应的火焰呈黄色,则原溶液最后一定含有钠离子,据此进行判断.
解答 解:溶液A通入过量氯水、和过量的碳酸铵溶液后生成白色沉淀甲,该白色沉淀只能为氢氧化铝,氢氧化铁沉淀为红褐色,则原溶液最后一定不存在Fe2+、Fe3+,原溶液最后一定含有Al3+,根据离子共存可知一定不存在SO32-、CO32-,则生成的气体甲只能为二氧化碳气体;向溶液甲中通入氢氧化钡溶液后生成白色沉淀乙,由于碳酸铵过量,白色沉淀乙中一定含有BaCO3,可能含有BaSO4,气体乙为氨气;溶液乙的焰色反应的火焰呈黄色,则原溶液最后一定含有钠离子,
A.白色沉淀乙中一定含有BaCO3,可能含有BaSO4,所以如果有硫酸钡则不溶,故A错误;
B.根据分析可知,溶液中一定存在Al3+、Na+,一定不存在SO32-、CO32-、Fe2+、Fe3+,故B正确;
C.可能有 K+、SO42-、Cl-,故C错误;
D.气体甲为二氧化碳,乙为氨气,二者都为无色、易溶于水的气体,二氧化碳无刺激性气味,故D错误;
故选B.
点评 本题考查了常见气体的性质及检验方法,题目难度中等,明确常见离子的性质为解答关键,注意掌握常见气体的检验方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
13.YBa2Cu8Ox(Y为元素钇)是磁悬浮列车中的重要超导材料,关于${\;}_{39}^{89}$Y的说法正确的是( )
| A. | Y在周期表中的位置是第4周期ⅢB族 | |
| B. | 属于非金属元素 | |
| C. | ${\;}_{39}^{89}$Y和${\;}_{39}^{89}$Y是两种不同的核素 | |
| D. | 核素${\;}_{39}^{89}$Y的质子数与中子数之差为50 |
10.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,2.24LH2O中分子的数目为0.1NA | |
| B. | 0.1mol•L-1NH4Cl溶液中含有Cl-的数目为0.1NA | |
| C. | 常温下,1.7gNH3中含有氢原子数目为0.3 NA | |
| D. | 5.6g铁粉在足量的氯气中充分燃烧,转移电子数为0.2NA |
7.pmolC2H4在密闭容器中加强热分解,达到平衡时生成mmolC2H2和nmolH2,将平衡混合气体完全燃烧生成水和二氧化碳,要消耗氧气( )
| A. | ($\frac{3m}{2}$+$\frac{n}{2}$+2p)mol | B. | (3p-$\frac{3m}{2}$-$\frac{n}{2}$)mol | C. | 3pmol | D. | ($\frac{3m}{2}$+$\frac{n}{2}$)mol |
14.①丁烷 ②2-甲基丙烷 ③戊烷 ④2-甲基丁烷 ⑤2,2-二甲基丙烷等物质的沸点按由高到低的排列顺序正确的是( )
| A. | ①>②>③>④>⑤ | B. | ⑤>④>③>②>① | C. | ③>①>④>②>⑤ | D. | ③>④>⑤>①>② |
11.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1 mol O2与Na完全反应,转移电子数一定为4NA | |
| B. | 22.4 L NH3中含有共价键的数目为3NA | |
| C. | 142 g Na2SO4和Na2HPO4混合物中含有的阴、阳离子总数是3NA | |
| D. | 标准状况下,11.2 L SO3所含的分子数目为0.5NA |
 .
.