题目内容
【题目】不同温度下水的离子积常数如表所示:
t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 100 |
KW/10﹣14 | 0.114 | 0.292 | 0.681 | 1.00 | 2.92 | 5.47 | 55.0 |
①请用文字解释随温度升高水的离子积增大的原因:
②25℃条件下,pH=4的盐酸溶液中由水电离出来的H+的浓度为mol/L
③10℃时纯水的电离平衡常数为 .
【答案】水电离吸热,升高温度后平衡正向移动;1.0×10﹣10;5.3×10﹣17
【解析】解:①水的电离是吸热反应,升高温度促进电离,所以水的离子积常数随着温度的升高而增大;所以答案是:水电离吸热,升高温度后平衡正向移动;②25℃条件下,水溶液中存在离子积常数Kw=10﹣14 , pH=4的盐酸溶液中由水电离出来的H+的浓度= ![]() =10﹣10mol/L,所以答案是:1.0×10﹣10; ③1L水的物质的量=
=10﹣10mol/L,所以答案是:1.0×10﹣10; ③1L水的物质的量= ![]() =55.6mol,10℃时纯水的电离平衡常数Ka=
=55.6mol,10℃时纯水的电离平衡常数Ka= ![]() =
= ![]() =5.3×10﹣17 , 所以答案是:5.3×10﹣17 .
=5.3×10﹣17 , 所以答案是:5.3×10﹣17 .

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
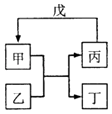
【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足如图转化关系的是( )
甲 | 乙 | 丙 | 戊 | |
① | SiO2 | NaOH | Na2SiO3 | CO2 |
② | Fe | H2O | Fe2O3 | H2 |
③ | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | 过量CO2 |
④ | Na2O2 | CO2 | O2 | Na |
A.①③
B.①②
C.②④
D.①④