题目内容
7.某金属氯化物MCl2 40.5g,含有0.6mol Cl-,则金属M的摩尔质量为( )| A. | 135 g•mol-1 | B. | 99.5g•mol-1 | C. | 67.5 g•mol-1 | D. | 64 g•mol-1 |
分析 含有0.6mol Cl-,则n(MCl2)=$\frac{0.6mol}{2}$=0.3mol,结合M=$\frac{m}{n}$计算.
解答 解:含有0.6mol Cl-,则n(MCl2)=$\frac{0.6mol}{2}$=0.3mol,M(MCl2)=$\frac{40.5g}{0.3mol}$=135g/mol,则金属M的摩尔质量为135g/mol-35.5g/mol×2=64 g•mol-1,
故选D.
点评 本题考查物质的量的计算,为高频考点,把握物质的构成、物质的量与质量的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
相关题目
11. 科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )
科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )
 科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )
科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )| A. | 烃X的分子式为C5H4 | |
| B. | 分子中碳原子的化学环境有2种 | |
| C. | 具有2个三元环的X的同分异构体共2种(含本身) | |
| D. | X分子中只有碳碳单键,没有碳碳双键 |
15.下列反应中生成物的总能量大于反应物的总能量的是( )
| A. | 铝粉与氧化铁的反应 | B. | 氯化铵与Ba(OH)2•8H2O反应 | ||
| C. | 锌片与稀硫酸反应 | D. | 钠与冷水反应 |
2.对于可逆反应,FeCl3+3KSCN?Fe(SCN)3(红色)+3KCl,达到平衡后,下列叙述正确的是( )
| A. | 加入FeCl3浓溶液或固体后,溶液颜色加深 | |
| B. | 加入少量KCl固体,增大了生成物浓度,平衡向逆反应方向移动,溶液颜色变浅 | |
| C. | 滴加几滴NaOH溶液,有红褐色沉淀生成,溶液颜色加深 | |
| D. | 加入几滴AgNO3溶液,有白色沉淀生成,溶液颜色加深 |
12.下列离子方程式书写正确的是( )
| A. | 将H2O2滴加到酸性KMnO4溶液中:2MnO4-+H2O2+6H+=2Mn2++3O2↑+4H2O | |
| B. | 在NH4HSO4溶液中慢慢滴入等物质的量的NaOH溶液:NH4++OH-→NH3•H2O | |
| C. | 用惰性电极电解氯化钠溶液:2H++2Cl-═H2↑+Cl2↑ | |
| D. | 用酸性高锰酸钾溶液滴定草酸:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O |
19.下列措施或事实不能用勒夏特列原理解释的是( )
| A. | 工业合成氨生产中增大压强 | |
| B. | 在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化 | |
| C. | NO2气体加压后颜色先变深再变浅 | |
| D. | 工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
16.下列说法正确的是( )
| A. | 6g 12C中约含有3.01×1023个碳原子 | |
| B. | 1 mol任何物质都含有6.02×1023个分子 | |
| C. | 1 mol O2的质量是32 g•mol-1 | |
| D. | 64 g氧相当于2 mol氧 |
17.臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g)?N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是( )
| A | B | C | D |
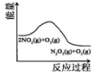 | 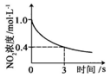 |  | 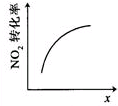 |
| 升高温度,平衡常数 减小 | 0~3s内,反应速率为v(NO2)=0.2mol•L-1•s-1 | t1时仅加入催化剂,平 衡向正方向移动 | 达平衡时,仅改变x, 则x为c(O2) |
| A. | A | B. | B | C. | C | D. | D |
 某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案.回答下列问题:
某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案.回答下列问题: