题目内容
12.下列离子方程式书写正确的是( )| A. | 将H2O2滴加到酸性KMnO4溶液中:2MnO4-+H2O2+6H+=2Mn2++3O2↑+4H2O | |
| B. | 在NH4HSO4溶液中慢慢滴入等物质的量的NaOH溶液:NH4++OH-→NH3•H2O | |
| C. | 用惰性电极电解氯化钠溶液:2H++2Cl-═H2↑+Cl2↑ | |
| D. | 用酸性高锰酸钾溶液滴定草酸:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O |
分析 A.2mol高锰酸根离子完全反应转移10个电子,生成5mol氧气,该反应不满足电子守恒;
B.物质的量相等时,氢离子优先反应,铵根离子不反应;
C.电解的是氯化钠溶液,水不能拆开;
D.酸性高锰酸钾溶液具有强氧化性,能够将草酸氧化成二氧化碳.
解答 解:A.将H2O2滴加到酸性KMnO4溶液中,二者是氧化还原反应,正确的离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,故A错误;
B.刘淑晴阿登与氢氧化钠的物质的量相等时,氢离子结合氢氧根离子的能力较强,所以只有氢离子反应,正确的离子方程式为:H++OH-=H2O,故B错误;
C.用惰性电极电解氯化钠溶液,反应生成氢气、氯气和氢氧化钠,正确的离子方程式为:2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH-,故C错误;
D.用酸性高锰酸钾溶液滴定草酸:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
15.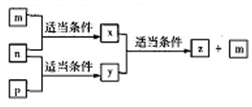 A、B、C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、p、n分别是元素A、B、C的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且x是用于配制饮料,它们之间有如图转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )
A、B、C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、p、n分别是元素A、B、C的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且x是用于配制饮料,它们之间有如图转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )
 A、B、C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、p、n分别是元素A、B、C的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且x是用于配制饮料,它们之间有如图转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )
A、B、C、D四种原子序数依次增大的分别位于三个不同短周期的主族元素,m、p、n分别是元素A、B、C的单质,x、y、z是由A、B、C组成的二元化合物,其中y、z是气体且x是用于配制饮料,它们之间有如图转化关系,D的单质可与热水发生置换反应,下列说法正确的是( )| A. | D的单质起火燃烧时可用x作灭火剂 | |
| B. | 元素的非金属性:C>A>B>D | |
| C. | B、C、D与A形成的简单化合物的熔点:C>D>B | |
| D. | 原子半径:D>B>C>A |
3.下列说法正确的是( )
| A. | 某试样焰色反应呈黄色,该试样中可能存在K+ | |
| B. | 广泛pH试纸测得某新制氯水的pH值为4 | |
| C. | 配制240mL 1mol/L NaOH溶液应称取NaOH固体9.6g | |
| D. | 可用排饱和食盐水来收集纯净的氯气 |
20.下列有关化学用语表示正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | NH3的电子式: | ||
| C. | 过氧化氢的电子式: | D. | 乙酸的球棍模型: |
7.某金属氯化物MCl2 40.5g,含有0.6mol Cl-,则金属M的摩尔质量为( )
| A. | 135 g•mol-1 | B. | 99.5g•mol-1 | C. | 67.5 g•mol-1 | D. | 64 g•mol-1 |
17.下列表示正确的是( )
| A. | 氯化钠的电子式: | B. | 二氧化碳的结构式:O-C-O | ||
| C. | S2-的结构示意图: | D. | 葡萄糖的分子式:C6H12O6 |
1.能正确表示下列反应的离子方程式是( )
| A. | 稀盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 钠与硝酸铜溶液反应:2Na+Cu2+=Cu+2Na+ | |
| C. | KHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 醋酸钠水解:CH3COO-+H2O?CH3COOH+OH- |
