题目内容
17.臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g)?N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是( )| A | B | C | D |
 |  |  |  |
| 升高温度,平衡常数 减小 | 0~3s内,反应速率为v(NO2)=0.2mol•L-1•s-1 | t1时仅加入催化剂,平 衡向正方向移动 | 达平衡时,仅改变x, 则x为c(O2) |
| A. | A | B. | B | C. | C | D. | D |
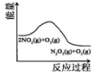
分析 A、由图可知,反应物总能量高于生成物总能量,正反应为放热反应,升高温度平衡向逆反应方向移动;
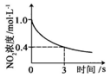
B、根据v=$\frac{△c}{△t}$进行计算求解;
C、使用催化剂,反应速率加快,但平衡不移动;
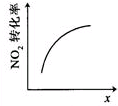
D、达平衡时,仅增大c(O2),平衡向逆反应方向移动,二氧化氮转化率降低.
解答 解:A、由图可知,反应物总能量高于生成物总能量,正反应为放热反应,升高温度平衡向逆反应方向移动,平衡常数减小,故A正确;
B、0~3s内,反应速率为v(NO2)=$\frac{1-0.4}{3}$=0.2mol•L-1•s-1,故B正确;
C、t1时刻,改变条件,反应速率加快,平衡不移动,该反应前后气体的物质的量减小,不能是增大压强,只能是使用催化剂,但催化剂不影响平衡的移动,故C错误;D、达平衡时,仅增大c(O2),平衡向逆反应方向移动,二氧化氮转化率降低,由图可知,二氧化氮的转化率随x增大而增大,x可以代表O3浓度、压强,故D错误;
故选:AB.
点评 本题以图象形式,考查化学反应中能量变化、化学反应速率计算、化学平衡图象及影响因素等,难度中等.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
7.某金属氯化物MCl2 40.5g,含有0.6mol Cl-,则金属M的摩尔质量为( )
| A. | 135 g•mol-1 | B. | 99.5g•mol-1 | C. | 67.5 g•mol-1 | D. | 64 g•mol-1 |
5.下列说法中,不正确的是( )
| A. | 冰融化,克服的是H2O的分子间作用力 | |
| B. | 同分异构现象存在,是有机化合物种类繁多的原因之一 | |
| C. | 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成 | |
| D. | Na2 O2属于离子化合物,该物质中存在离子键和共价键 |
12.海洋中有丰富的食品、矿产、能源、药物和水产等资源,如图表示海水综合利用的部分过程.下列说法不正确的是( )
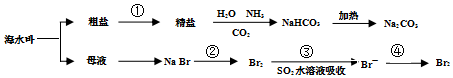

| A. | 工业上通过电解熔融状态MgCl2制取金属镁 | |
| B. | 用澄清石灰水可鉴别NaHCO3和Na2CO3 | |
| C. | 在第②、④步骤中,溴元素均被氧化 | |
| D. | 制取NaHCO3的反应中,利用了其溶解度在相同条件下小于NaCl的性质 |
9.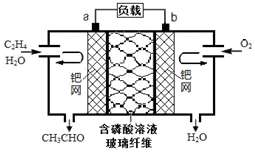 乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )
乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )
 乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )
乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )| A. | 该电池可实现化学能与电能的相互转化 | |
| B. | 电子移动方向:电极a→磷酸溶液→电极b | |
| C. | 放电时,电路中每转移0.4mol电子,溶液中就有0.4molH+向负极迁移 | |
| D. | 该电池的负极反应式为:CH2═CH2-2e-+H2O=CH3CHO+2H+ |
11.下列各组离子一定能大量共存的是( )
| A. | 在强碱性溶液中:Na+、K+、[Al(OH)4]-、CO32- | |
| B. | 在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| C. | 在c(H+)=10-13mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |

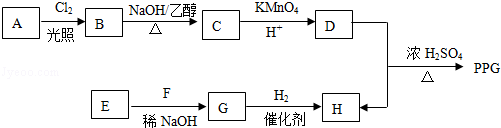
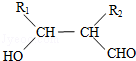
 .
.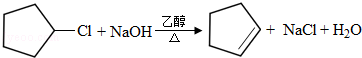 .
.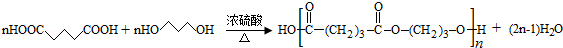 .
.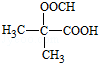 (写构简式)
(写构简式)