题目内容
2013年2月朝鲜进行了第三次核试验,引起国际社会的极大关注.
U是一种重要的核燃料,这里的“235”是指该原子的( )
235 92 |
| A、质量数 | B、质子数 |
| C、中子数 | D、电子数 |
考点:核素
专题:原子组成与结构专题
分析:根据原子符号左上角数字表示质量数,左下角数字表示质子数来解答.
解答:
解:235U中“235”是指该原子的质量数,故选:A.
点评:本题主要考查了原子符号的含义,元素符号的左下角是质子数、左上角是质量数,质量数=质子数+中子数,属于基础知识考查,较简单.

练习册系列答案
相关题目
化学与生产、生活密切相关,下列叙述错误的是( )
| A、用热的纯碱溶液清除灶具上的油污 |
| B、用硫酸清洗锅炉中的水垢 |
| C、用明矾[KAl(SO4)2.12H2O]作净水剂,除去水中悬浮的杂质 |
| D、用Na2S作沉淀剂,除去废水中的Cu2+和Hg2+ |
钠元素与硅元素最本质的区别是( )
| A、质子数不同 |
| B、相对原子质量不同 |
| C、中子数不同 |
| D、最外层电子数不同 |
下列反应能用CO32-+2H+═CO2↑+H2O表示的是( )
| A、Na2CO3+H2SO4═Na2SO4+CO2↑+H2O |
| B、CaCO3+2HCl═CaCl2+CO2↑+H2O |
| C、KHCO3+HCl═KCl+CO2↑+H2O |
| D、BaCO3+2HNO3═Ba(NO3 )2+CO2↑+H2O |
下列化学用语正确的是( )
| A、H2O的结构式:H-O-H |
| B、乙醇的结构简式:C2H6O |
C、H2O2的电子式: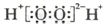 |
D、14C的原子结构示意图: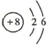 |
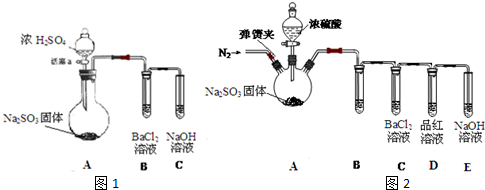
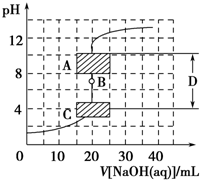 滴定法是中学化学中一种十分重要的定量分析方法.滴定法又可进一步分为酸碱中和滴定、氧化还原滴定等若干种.
滴定法是中学化学中一种十分重要的定量分析方法.滴定法又可进一步分为酸碱中和滴定、氧化还原滴定等若干种.