题目内容
下列物质的性质、用途正确的是( )
| A、浓硫酸、浓硝酸都具有强氧化性,不能盛放在金属容器中 |
| B、明矾和漂白粉常用于自来水的净化,两者的作用原理完全相同 |
| C、Na2SiO3是制备硅胶和木材防火剂的原料 |
| D、合金的硬度比纯金属大,熔点也比纯金属高 |
考点:浓硫酸的性质,硝酸的化学性质,含硅矿物及材料的应用,合金的概念及其重要应用,镁、铝的重要化合物
专题:元素及其化合物
分析:A.常温下,浓硫酸和浓硝酸与Al、Fe都发生钝化现象;
B.明矾的漂白原理是利用铝离子水解生成的氢氧化铝胶体的吸附性,漂白粉漂白原理是利用了次氯酸钙的强氧化性;
C.硅酸钠不燃烧也不支持燃烧,硅酸钠和稀盐酸反应生成硅酸;
D.合金的硬度大、熔点低.
B.明矾的漂白原理是利用铝离子水解生成的氢氧化铝胶体的吸附性,漂白粉漂白原理是利用了次氯酸钙的强氧化性;
C.硅酸钠不燃烧也不支持燃烧,硅酸钠和稀盐酸反应生成硅酸;
D.合金的硬度大、熔点低.
解答:
解:A.常温下,浓硫酸和浓硝酸与Al、Fe都发生钝化现象而阻止进一步反应,所以常温下,浓硫酸和浓硝酸可以用Fe或Al容器盛放,故A错误;
B.明矾的漂白原理是利用铝离子水解生成的氢氧化铝胶体的吸附性,漂白粉漂白原理是利用了次氯酸钙的强氧化性,两者的作用原理不相同,故B错误;
C.硅酸钠不燃烧也不支持燃烧,硅酸钠和稀盐酸反应生成难溶性的硅酸而制得硅胶,所以Na2SiO3是制备硅胶和木材防火剂的原料,故C正确;
D.合金的硬度比其成分都大、熔点比其成分都低,故D错误;
故选C.
B.明矾的漂白原理是利用铝离子水解生成的氢氧化铝胶体的吸附性,漂白粉漂白原理是利用了次氯酸钙的强氧化性,两者的作用原理不相同,故B错误;
C.硅酸钠不燃烧也不支持燃烧,硅酸钠和稀盐酸反应生成难溶性的硅酸而制得硅胶,所以Na2SiO3是制备硅胶和木材防火剂的原料,故C正确;
D.合金的硬度比其成分都大、熔点比其成分都低,故D错误;
故选C.
点评:本题考查物质的性质与用途,明确物质的性质是解本题关键,知道其使用原理,注意:钝化现象不是不反应,为易错点.

练习册系列答案
相关题目
(Ⅰ)1-溴丙烷与2-溴丙烷分别和氢氧化钠的醇溶液混和加热;(Ⅱ)1-溴丙烷与2-溴丙烷分别和氢氧化钠的水溶液混和加热,则下列说法正确的是( )
| A、(Ⅰ)(Ⅱ)产物均相同 |
| B、(Ⅰ)(Ⅱ)产物均不同 |
| C、(Ⅰ)产物相同,(Ⅱ)产物不同 |
| D、(Ⅰ)产物不同,(Ⅱ)产物相同 |
科学家P?Tatapudi等人首先使用在空气中电解水(酸性)的方法,在阳极制得臭氧,阴极制得过氧化氢.电解总方程式为:3H2O+3O2?3H2O2+O3,下列说法正确的是( )
| A、阳极反应:3O2+6e-+6H+=3H2O2 |
| B、氧化性:O2>O3 |
| C、电解一段时间后,溶液pH下降 |
| D、每转移3 mol电子,可生成标准状况下22.4 L O3 |
下列关于离子晶体的描述不正确的是( )
| A、离子晶体是阳离子和阴离子通过静电吸引力结合而成的晶体 |
| B、晶格能由大到小:NaF>NaCl>NaBr>NaI |
| C、硬度:MgO>CaO>BaO |
| D、在氯化钠晶体中,Na+和Cl-的配位数均为6 |
下列有关生活中化学的叙述错误的是( )
| A、向燃料煤中加入生石灰,可以减少对大气的污染 |
| B、用双氧水清洗伤口,可以杀菌消毒 |
| C、只用淀粉溶液就能检验出食盐中是否加碘 |
| D、随意丢弃废旧电池,会对环境造成污染 |
化学与生活、社会密切相关.下列有关说法中,不正确的是( )
| A、雾霾天气严重危害人体健康,而形成雾霾天气的“罪魁祸首”是PM2.5 |
| B、地沟油,潲水油在餐饮企业中不能使用,但却可以用于制肥皂,变废为宝 |
| C、天宫一号使用的碳纤维是一种新型无机高分子材 料 |
| D、纤维素能在人体内水解,生成的葡萄糖能为人体提供能量 |
下列事实,不能用勒沙特列原理解释的是( )
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO 当加入AgNO3溶液后,溶液颜色变浅 |
| B、合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施 |
| C、反应CO+NO2?CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 |
| D、对2HI(g)?H2(g)+I2(g),平衡体系增大压强可使颜色变深 |
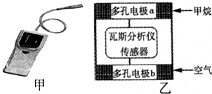 瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )
瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )| A、电极a的反应式为:CH4+4O2--8e-=CO2+2H2O |
| B、电极b是正极,O2-由电极b流向电极a |
| C、瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| D、当固体电解质中有1 molO2-通过时,电子转移2 mol |
下列各组离子一定能大量共存的是( )
| A、在无色溶液中:NH4+、Fe2+、SO42-、CO32- |
| B、加铝粉产生氢气的溶液中:NH4+、NO3?、Cl?、Ba2+ |
| C、在pH=1的溶液中:K+、Fe2+、Cl-、CH3COO- |
| D、含有0.1 mol?L-1H2SO4的溶液中:K+、Mg2+、Cl-、NO3- |