题目内容
下列关于离子晶体的描述不正确的是( )
| A、离子晶体是阳离子和阴离子通过静电吸引力结合而成的晶体 |
| B、晶格能由大到小:NaF>NaCl>NaBr>NaI |
| C、硬度:MgO>CaO>BaO |
| D、在氯化钠晶体中,Na+和Cl-的配位数均为6 |
考点:离子晶体
专题:化学键与晶体结构
分析:A、阴阳离子通过静电作用形成离子键;
B、所带电荷相等时,离子半径越小,晶格能越大;
C、根据原子半径大小比较键能,根据键能大小比较硬度;
D、依据氯化钠的晶胞结构分析即可.
B、所带电荷相等时,离子半径越小,晶格能越大;
C、根据原子半径大小比较键能,根据键能大小比较硬度;
D、依据氯化钠的晶胞结构分析即可.
解答:
解:A、阴阳离子通过静电作用所形成的化学键叫离子键,静电作用既有吸引又有排斥,故A错误;
B、四种物质所带电荷相同,由于离子半径:F-<Cl-<Br-<I-,因此晶格能:NaI<NaBr<NaCl<NaF,故B正确;
C、原子半径Ba>Ca>Mg,原子半径越大,键能越小,硬度越小,故C正确;
D、NaCl为立方面心结构,钠离子的配位数为6,Cl-的配位数是6,故D正确,
故选A.
B、四种物质所带电荷相同,由于离子半径:F-<Cl-<Br-<I-,因此晶格能:NaI<NaBr<NaCl<NaF,故B正确;
C、原子半径Ba>Ca>Mg,原子半径越大,键能越小,硬度越小,故C正确;
D、NaCl为立方面心结构,钠离子的配位数为6,Cl-的配位数是6,故D正确,
故选A.
点评:本题考查较为综合,涉及晶体的类型以及性质的判断,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
下列物质不是生活中常用的添加剂的是( )
| A、食盐 | B、面粉 | C、酱油 | D、味精 |
下列叙述正确的是( )
| A、晶体中只要有阳离子就一定有阴离子 |
| B、金刚石和冰在熔化时克服的作用力相同 |
| C、HCl晶体由H+和Cl-构成 |
| D、原子晶体里,所有原子都以共价键相互结合 |
下列有关元素的叙述正确的是( )
| A、所有主族非金属元素,都有最高正价且等于其最外层电子数 |
| B、单原子形成的离子,一定具有稀有气体原子的核外电子排布 |
| C、某元素原子最外层电子数有2个,则该元素一定是第ⅡA族的元素 |
| D、两种单原子,若核外电子排布完全相同,则一定属于同种元素 |
下列物质的性质、用途正确的是( )
| A、浓硫酸、浓硝酸都具有强氧化性,不能盛放在金属容器中 |
| B、明矾和漂白粉常用于自来水的净化,两者的作用原理完全相同 |
| C、Na2SiO3是制备硅胶和木材防火剂的原料 |
| D、合金的硬度比纯金属大,熔点也比纯金属高 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质.其工作原理如图所示:下列关于固体燃料电池的有关说法正确的是( )
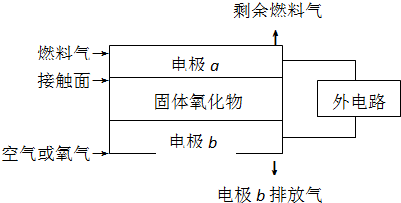

| A、电极b为电池负极,电极反应式为2O2+4e-=4O2- |
| B、固体氧化物的作用是让电子在电池内通过 |
| C、若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-=2H++H2O |
| D、若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-=2CO2+2H2O |