题目内容
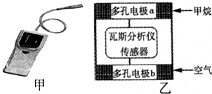 瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )
瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )| A、电极a的反应式为:CH4+4O2--8e-=CO2+2H2O |
| B、电极b是正极,O2-由电极b流向电极a |
| C、瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| D、当固体电解质中有1 molO2-通过时,电子转移2 mol |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.电子在外电路转移,通甲烷气体的为负极,通空气一端为正极,电池总反应为CH4+2O2=CO2+H2O,正极反应为:O2+4e-=2O2-,负极反应为:CH4+4O2--8e-=CO2+2H2O,结合原电池的原理和电极反应回答问题;
解答:
解:A、电极a为甲烷失电子,为负极,则电极a的反应式为:CH4+4O2--8e-=CO2+2H2O,故A正确;
B、电极b氧气得电子,生成O2-,而电极a需要O2-作为反应物,故O2-由正极(电极b)流向负极(电极a),故B正确;
C、电子不能在电池内电路流动,只能在外电路中流动,故C错误;
D、1mol O2得4mol电子生成2molO2-,故当固体电解质中有1mol O2-通过时,电子转移2mol,故D正确;
故选C.
B、电极b氧气得电子,生成O2-,而电极a需要O2-作为反应物,故O2-由正极(电极b)流向负极(电极a),故B正确;
C、电子不能在电池内电路流动,只能在外电路中流动,故C错误;
D、1mol O2得4mol电子生成2molO2-,故当固体电解质中有1mol O2-通过时,电子转移2mol,故D正确;
故选C.
点评:本题考查了化学电源新型电池的原电池原理应用,主要理解电池电解质不是在水溶液中的氧化还原反应,电解质是固体,O2-可以在其中自由移动,是本题的关键.

练习册系列答案
相关题目
下列物质的性质、用途正确的是( )
| A、浓硫酸、浓硝酸都具有强氧化性,不能盛放在金属容器中 |
| B、明矾和漂白粉常用于自来水的净化,两者的作用原理完全相同 |
| C、Na2SiO3是制备硅胶和木材防火剂的原料 |
| D、合金的硬度比纯金属大,熔点也比纯金属高 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质.其工作原理如图所示:下列关于固体燃料电池的有关说法正确的是( )
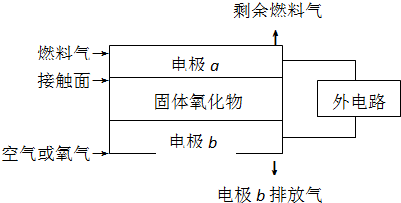

| A、电极b为电池负极,电极反应式为2O2+4e-=4O2- |
| B、固体氧化物的作用是让电子在电池内通过 |
| C、若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-=2H++H2O |
| D、若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-=2CO2+2H2O |
下列化学用语表示正确的是( )
| A、Na+的电子排布式:1s22s22p63s1 |
| B、Fe的简化电子排布式:[Ar]4s2 |
| C、Cr的外围电子排布式:3d54s1 |
D、N的最外层电子排布图: |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸汽和硫固体分别完全燃烧,前者放出热量比后者少 |
| B、由C(石墨)=C(金刚石);△H=+1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| C、在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=-571.6 kJ?mol-1 |
| D、在稀溶液中,H+(aq)+OH-(aq)═H2O(1);△H=一57.3 kJ?mol-1,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ |
等物质的量的CH4和NH3相比较,下列结论错误的是?( )
| A、它们的分子个数比为1:1 |
| B、它们的原子个数比为5:4 |
| C、它们的电子个数比为1:1 |
| D、它们的体积比为1:1 |
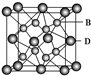 有A、B、C、D、E五种元素,其相关信息如下:
有A、B、C、D、E五种元素,其相关信息如下: