��Ŀ����
13��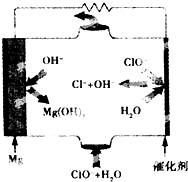 þȼ�ϵ�ؾ��б������ߡ�ʹ�ð�ȫ���㡢ԭ������Դ�ḻ���ɱ��͡�ȼ���������˼���ȾС���ص㣮��ͼΪþ--��������ȼ�ϵ�صĹ���ԭ��ͼ�������й�˵������ȷ���ǣ�������
þȼ�ϵ�ؾ��б������ߡ�ʹ�ð�ȫ���㡢ԭ������Դ�ḻ���ɱ��͡�ȼ���������˼���ȾС���ص㣮��ͼΪþ--��������ȼ�ϵ�صĹ���ԭ��ͼ�������й�˵������ȷ���ǣ�������| A�� | ���ܷ�ӦʽΪMg+ClO-+H2O=Mg��OH��2��+Cl- | |
| B�� | ������ӦʽΪClO-+H2O+2e-=Cl-+2OH- | |
| C�� | ��ȼ�ϵ����þΪ������������ԭ��Ӧ�� | |
| D�� | �ŵ������OH-���� |
���� ��ȼ�ϵ���У�þ��ʧ����������������������ӵõ��ӷ�����ԭ��Ӧ�������缫��ӦʽΪMg-2e-=Mg 2+�������缫��ӦʽΪ��ClO-+H2O+2e-=Cl-+2OH-���ŵ�ʱ���������Һ�����������ƶ���
��� �⣺A��þ�ڸ�����ʧ��������þ���ӣ�������������������ϵõ��Ӻ�ˮ���������Ӻ����������ӣ����Ե�ط�ӦʽΪMg+ClO-+H2O=Mg��OH��2+Cl-����A��ȷ��
B��������˫��ˮ�õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪClO-+H2O+2e-�TCl-+2OH-����B��ȷ��
C��þʧ���ӷ���������Ӧ������������C����
D���ŵ�������������������ƶ�����D��ȷ��
��ѡC��
���� ���⿼����ԭ���ԭ������ȷ�������Ϸ����ķ�Ӧ�ǽⱾ��ؼ����ٽ�������ƶ����������������Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
�����Ŀ
3������̼��һ����Ҫ�ġ����ײ��ϡ���������ֱ��Ϊ1��100nm֮�䣮��������̼���ȵط�ɢ������ˮ�У����γɵķ�ɢϵ�ǣ�����Һ���ڽ��塡���ܲ��������ЧӦ����������ֽ����������Ĥ�����û�������ɫ������������ȷ���ǣ�������
| A�� | �ڢݢ� | B�� | �ڢۢݢ� | C�� | �ڢۢ� | D�� | �٢ۢ� |
18�����й������ʻ����Ӽ����������ȷ���ǣ�������
| A�� | ����Һ�м�KSCN����Һ�Ժ�ɫ��֤��ԭ��Һ����Fe3+����Fe2+ | |
| B�� | ����Һ�еμ������ữ���ڵμ����ᱵ��Һ�����а�ɫ������������SO42- | |
| C�� | ���հ�ɫ��ĩ������ɻ�ɫ��֤��ԭ��ĩ����Na+����K+ | |
| D�� | ������ͨ�����ʯ��ˮ����Һ����ǣ�֤��ԭ���������CO2 |
5��������Һ���Ƿ���Fe3+�����õ��Լ��ǣ�������
| A�� | ϡHCl | B�� | ������Һ | C�� | KSCN ��Һ | D�� | NaCl ��Һ |
3����ұ�������ȼ���״������һ����ҵ������ͼ��ʾ��������������Դ�������ʣ����ٻ�����Ⱦ��
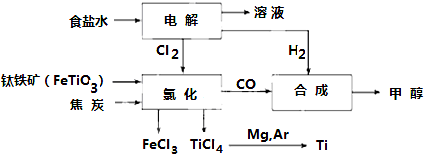
��ش��������⣺
��1��Feλ��Ԫ�����ڱ��е������ڵ�VIII�壮
��2��д���������ڸ������뽹̿���Ȼ��õ����Ȼ��ѵĻ�ѧ����ʽ2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2FeCl3+2TiCl4+6CO
��3���Ʊ�TiO2�ķ���֮һ������TiCl4ˮ������TiO2•xH2O���پ������Ƶã�д��TiCl4ˮ��Ļ�ѧ����ʽ��TiCl4+��2+x��H2O=TiO2��xH2O��+4HCl��
��4����Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ�������ķ�������õ�Ti�������±���Ϣ������ȵ��¶��Ը���1412�漴�ɣ�
��5�����ʳ��ˮ�����ӷ���ʽ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����

��ش��������⣺
��1��Feλ��Ԫ�����ڱ��е������ڵ�VIII�壮
��2��д���������ڸ������뽹̿���Ȼ��õ����Ȼ��ѵĻ�ѧ����ʽ2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2FeCl3+2TiCl4+6CO
��3���Ʊ�TiO2�ķ���֮һ������TiCl4ˮ������TiO2•xH2O���پ������Ƶã�д��TiCl4ˮ��Ļ�ѧ����ʽ��TiCl4+��2+x��H2O=TiO2��xH2O��+4HCl��
��4����Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ�������ķ�������õ�Ti�������±���Ϣ������ȵ��¶��Ը���1412�漴�ɣ�
| TiCl4 | Mg | MgCl2 | Ti | |
| �۵�/�� | -25.0 | 648.8 | 714 | 1667 |
| �е�/�� | 136.4 | 1090 | 1412 | 3287 |

 ��
��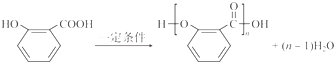 ��
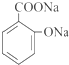
��
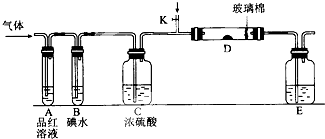 ijС�������ͼ��ʾ��װ��ͼ��ͼ�мгֺͼ���װ����ȥ�����ֱ��о�S02��Cl2�����ʣ�
ijС�������ͼ��ʾ��װ��ͼ��ͼ�мгֺͼ���װ����ȥ�����ֱ��о�S02��Cl2�����ʣ� ���������ḻ��ʣ�����Ľṹ�����ӣ��˽̰�γ̱����н̲ġ�ѡ��3��������չʾ��һЩ���;���Ľṹ�����ʵ����֪ʶ���磺�ɱ����������ʯ��ʯī���ǡ��ء�þ��ͭ��NaCl��CsCl��CaF2����ͼ��һ����������ͼ�������������������ʷ�Χ�ڻش��������⣺
���������ḻ��ʣ�����Ľṹ�����ӣ��˽̰�γ̱����н̲ġ�ѡ��3��������չʾ��һЩ���;���Ľṹ�����ʵ����֪ʶ���磺�ɱ����������ʯ��ʯī���ǡ��ء�þ��ͭ��NaCl��CsCl��CaF2����ͼ��һ����������ͼ�������������������ʷ�Χ�ڻش��������⣺