题目内容
6.设NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 0.5molAl与足量盐酸反应转移电子数为1NA | |
| B. | 标准状况下,22.4L氨气与22.4L氮气所含原子数均为2NA | |
| C. | 7.8gNa2O2所含的离子数为0.3NA | |
| D. | 11.2LCl2完全溶于NaOH溶液,电子转移数为0.5NA |
分析 A.0.5mol铝与足量盐酸反应生成0.5mol氯化铝,转移了1.5mol电子;
B.氨气分子中含有4个原子,氮气分子中含有2个原子;
C.过氧化钠中含有的阴离子为过氧根离子,7.8g过氧化钠的物质的量为0.1mol,含有0.2mol钠离子和0.1mol过氧根离子;
D.没有告诉在标准状况下,不能使用标准状况下的气体摩尔体积计算氯气的物质的量.
解答 解:A.Al为+3价金属,0.5molAl与足量盐酸反应转移了1.5mol电子,转移电子数为1.5NA,故A错误;
B.标准状况下22.4L气体的物质的量为1mol,1mol氨气分子中含有4mol原子,1mol氮气分子中含有2mol原子,二者含有的原子数不相等,故B错误;
C.7.8g过氧化钠的物质的量为0.1mol,0.1mol过氧化钠中含有0.2mol钠离子和0.1mol过氧根离子,所含的离子数为0.3NA,故C正确;
D.不是标准状况下,不能使用标准状况下的气体摩尔体积计算11.2L氯气的物质的量,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意明确标准状况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,D为易错点,注意没有告诉在标准状况下.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
16.下列叙述或变化,不能用勒夏特列原理解释的是( )
| A. | 红棕色的NO2,加压后颜色先变深后变浅 | |
| B. | 高压比常压有利于合成SO3的反应 | |
| C. | 加入催化剂有利于氨的合成 | |
| D. | 工业制取金属钾的反应为:Na(l)+KCl(l)?NaCl(l)+K(g) |
17.将一小块钠放入下列溶液时,不会出现沉淀的是( )
| A. | 氯化镁溶液 | B. | 饱和氢氧化钠溶液 | ||
| C. | 硫酸铜溶液 | D. | 稀硫酸 |
14.下列化学用语表达正确的是( )
①丙烷的球棍模型: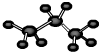
②丙烯的结构简式为:CH3CHCH2
③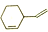 的化学式为C8H12
的化学式为C8H12
④一氯甲烷和二氯甲烷、乙烯和苯乙烯互为同系物
⑤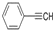 与C8H6互为同分异构体
与C8H6互为同分异构体
⑥石油是混合物,其分馏产品煤油为纯净物.
①丙烷的球棍模型:

②丙烯的结构简式为:CH3CHCH2
③
 的化学式为C8H12
的化学式为C8H12 ④一氯甲烷和二氯甲烷、乙烯和苯乙烯互为同系物
⑤
 与C8H6互为同分异构体
与C8H6互为同分异构体⑥石油是混合物,其分馏产品煤油为纯净物.
| A. | ①③④⑤ | B. | ①③ | C. | ②④⑥ | D. | ①② |
1.下列实验能达到目的是( )
| A. | 加热FeCl3溶液至沸腾制备Fe(OH)3胶体 | |
| B. | 用Ba(OH)2溶液鉴别Na2CO3和NaHCO3 | |
| C. | 用分液漏斗分离I2和CCl4的混合物 | |
| D. | 通过蒸馏可除去自来水中的Cl-等杂质而制取蒸馏水 |
11.下列现象说明SO2具有氧化性的是( )
| A. | SO2通入酸性高锰酸钾溶液中使之褪色 | |
| B. | SO2通入石蕊试液中使之变红色 | |
| C. | SO2通入氯水中使之褪色 | |
| D. | SO2通入饱和H2S溶液中析出浅黄色沉淀 |
15.下列关于化合物CH3-CH=CH-C≡C-CF3分子结构的叙述中正确的是( )
| A. | 6个碳原子有可能都在一条直线上 | B. | 有5个碳原子可能在一条直线上 | ||
| C. | 6个碳原子一定都在同一平面上 | D. | 6个碳原子不可能在同一平面上 |
11.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 54 g Al分别与足量的稀硫酸及氢氧化钠溶液反应失去的电子数都是6NA | |
| B. | 同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等 | |
| C. | 1 mol•L-1的MgCl2溶液中,含有Cl-个数为2NA | |
| D. | 11.2 L氧气中所含有的原子数为NA |