题目内容
3.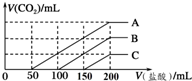 浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积(标准状况下)与所加盐酸体积之间关系如图所示.下列判断正确的是( )
浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积(标准状况下)与所加盐酸体积之间关系如图所示.下列判断正确的是( )| A. | 通入CO2后,A烧杯中的溶质成分是Na2CO3 | |
| B. | B烧杯中通入的CO2体积为448 mL | |
| C. | 原NaOH溶液的浓度为0.2 mol/L | |
| D. | 通入CO2后,C烧杯中溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:2 |
分析 A.若溶质只有Na2CO3,加入盐酸开始发生反应:Na2CO3+HCl=NaHCO3+NaCl,然后发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,前后两阶段消耗盐酸体积之比为1:1,而实际消耗盐酸体积为50:(200-50)=1:3,故溶质为Na2CO3、NaHCO3;
B.由图可知,曲线B中从100mL~200mL发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,根据消耗的盐酸计算生成二氧化碳的体积,根据碳原子守恒可知该反应生成的二氧化碳体积等于通入的二氧化碳的体积;
C.由图可知,加入200mLHCl时,产生二氧化碳的体积最大,说明此时溶液中溶质为NaCl,根据氯离子、钠离子守恒计算原溶液中氢氧化钠的物质的量,再根据c=$\frac{n}{V}$计算;
D.曲线C中,前后两消耗盐酸体积之比为3:1,结合A的分析可知,原NaOH溶液中通入CO2后,所得溶液中的溶质成分NaOH、Na2CO3,加入200mLHCl时,产生二氧化碳的体积最大,说明此时溶液中溶质为NaCl,根据碳原子守恒计算n(Na2CO3),根据钠离子守恒n(NaOH).
解答 解:A.若溶质只有Na2CO3,加入盐酸开始发生反应:Na2CO3+HCl=NaHCO3+NaCl,然后发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,前后两阶段消耗盐酸体积之比为1:1,而实际消耗盐酸体积为50:(200-50)=1:3,故溶质为Na2CO3、NaHCO3,故A错误;
B.由图可知,曲线B中从100mL~150mL发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,生成二氧化碳最大时,该阶段消耗盐酸为200mL-100mL=100mL,由方程式可知n(CO2)=n(HCl)=0.1L×0.2mol/L=0.02mol,V(CO2)=0.02mol×22.4L/mol=0.448L=448mL,根据碳原子守恒可知该反应生成的二氧化碳体积等于通入的二氧化碳的体积,即通入的二氧化碳为448mL,故B正确;
C.由图可知,加入200mLHCl时,产生二氧化碳的体积最大,说明此时溶液中溶质为NaCl,根据氯离子、钠离子守恒可得n(NaOH)=n(NaCl)=n(HCl)=0.2L×0.2mol/L=0.04mol,故原溶液中氢氧化钠的物质的量浓度=$\frac{0.04mol}{0.1L}$=0.4mol/L,故C错误;
D.曲线C中,前后两消耗盐酸体积之比为3:1,结合A的分析可知,原NaOH溶液中通入CO2后,所得溶液中的溶质成分NaOH、Na2CO3,产生二氧化碳消耗盐酸为200mL-150mL=50mL,由方程式可知n(CO2)=n(HCl)=0.05L×0.2mol/L=0.01mol,根据原子守恒可知n(Na2CO3)=n(CO2)=0.01mol,根据钠离子守恒n(NaOH)=0.04mol-2×0.01mol=0.02mol,故原NaOH溶液中通入CO2后,所得溶液中的n(NaOH):n(Na2CO3)=0.02mol:0.01mol=2:1,故D错误,
故选:B.
点评 本题考查混合物的有关计算、化学反应图象等,难度中等,根据图中盐酸的体积判断产生二氧化碳前CO2与NaOH反应过程是解题关键,注意守恒思想与方程式的运用.

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案| A. | 在28 g聚乙烯树脂中,含有的碳原子数目为2NA | |
| B. | 在合成28 g聚乙烯树脂的单体中,含有的双键数目为NA | |
| C. | 28 g聚乙烯树脂完全燃烧时,转移的电子数目为3NA | |
| D. | 28 g聚乙烯树脂中,含有的C-H键的数目为4NA |
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | Mg条插入NaOH溶液中 | 有气泡产生 | Mg可以和NaOH溶液反应 |
| B | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰无紫色 | 原溶液中无K+ |
| C | 用玻璃棒蘸取氨水点到红色石蕊试纸上 | 试纸变蓝色 | 氨水呈碱性 |
| D | CO2通入CaCl2水溶液中 | 溶液变浑浊 | 生成CaCO3沉淀 |
| A. | A | B. | B | C. | C | D. | D |
| A. | H+、Fe2+、NO3-、SO42- | B. | Al3+、NO3-、SO42-、AlO2- | ||
| C. | OH-、HCO3-、Cl-、K+ | D. | Fe3+、K+、SCN-、Cl- |
| A. | AgNO3 | B. | Ca(OH)2 | C. | Na2SO3 | D. | AlCl3 |
| A. | 0.1mol•L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3 mol•L-1 | |
| B. | 常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):③>②>① | |
| C. | 常温下将醋酸钠、盐酸两溶液混合后溶液呈中性,则混合溶液中:c(Na+)>c(Cl-)>c(CH3COOH) | |
| D. | 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数:N前>N后 |