题目内容
将浓度为0.1mol?L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A、c(H+) | ||
| B、K(HF) | ||
C、
| ||
D、
|
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A、HF为弱酸,则浓度为0.1mol?L-1HF溶液加水不断稀释,促进电离,但c(H+)不断减小;
B、电离平衡常数只与温度有关;
C、稀释时一段时间电离产生等量的H+和F-,溶液的体积相同,则两种离子的浓度的比值不变,但随着稀释的不断进行,c(H+)不会超过10-7mol?L-1,c(F-)不断减小,则比值变小;
D、根据Ka(HF)=
,当HF溶液加水不断稀释,分析
的变化.
B、电离平衡常数只与温度有关;
C、稀释时一段时间电离产生等量的H+和F-,溶液的体积相同,则两种离子的浓度的比值不变,但随着稀释的不断进行,c(H+)不会超过10-7mol?L-1,c(F-)不断减小,则比值变小;
D、根据Ka(HF)=
| c(F-)×c(H+) |
| c(HF) |
| c(H+) |
| c(HF) |
解答:
解:A、因HF为弱酸,则浓度为0.1mol?L-1HF溶液加水不断稀释,促进电离,平衡正向移动,电离程度增大,n(H+)增大,但c(H+)不断减小,故A错误;
B、因电离平衡常数只与温度有关,则Ka(HF)在稀释过程中不变,故B错误;
C、因稀释时一段时间电离产生等量的H+和F-,溶液的体积相同,则两种离子的浓度的比值不变,但随着稀释的不断进行,c(H+)不会超过10-7mol?L-1,c(F-)不断减小,则比值变小,故C错误;
D、因Ka(HF)=
,当HF溶液加水不断稀释,促进电离,c(F-)不断减小,Ka(HF)不变,则
增大,故D正确;
故选D.
B、因电离平衡常数只与温度有关,则Ka(HF)在稀释过程中不变,故B错误;
C、因稀释时一段时间电离产生等量的H+和F-,溶液的体积相同,则两种离子的浓度的比值不变,但随着稀释的不断进行,c(H+)不会超过10-7mol?L-1,c(F-)不断减小,则比值变小,故C错误;
D、因Ka(HF)=
| c(F-)×c(H+) |
| c(HF) |
| c(H+) |
| c(HF) |
故选D.
点评:本题考查弱电解质的稀释,明确稀释中电离程度、离子浓度、Ka的变化即可解答,本题难点和易错点是不断稀释时c(H+)不会超过10-7mol?L-1.

练习册系列答案
相关题目
一溴代烃A经水解后再氧化得到有机化合物B,A的一种同分异构体经水解得到有机化合物C,B和C可发生酯化反应生成酯D,则D可能是( )
| A、(CH3)2CHCOOC(CH3)3 |
| B、(CH3)2CHCOOCH2CH(CH3)2 |
| C、(CH3)2CHCOOCH(CH3)CH2CH3 |
| D、CH3(CH2)2COOCH2(CH2)2CH3 |
在一定条件下,同一物质中不能自身相互发生反应的是( )
| A、乙醇 | B、氨基酸 |
| C、乙烯 | D、硬脂酸 |
甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是( )
①甲由水电离出来的H+的物质的量浓度是乙的
倍
②物质的量浓度c(甲)=10c(乙)
③中和等物质的量的NaOH溶液需甲、乙两杯酸的体积,10V(甲)=V(乙)
④甲中的c(OH-)为乙中的c(OH-)的10倍.
①甲由水电离出来的H+的物质的量浓度是乙的
| 1 |
| 10 |
②物质的量浓度c(甲)=10c(乙)
③中和等物质的量的NaOH溶液需甲、乙两杯酸的体积,10V(甲)=V(乙)
④甲中的c(OH-)为乙中的c(OH-)的10倍.
| A、①②④正确 | B、①③正确 |
| C、②④正确 | D、只有①正确 |
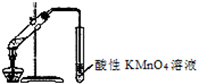 下列实验操作或实验方案设计正确的有.( )
下列实验操作或实验方案设计正确的有.( )①利用盐析分离提纯蛋白质.
②用酸性KMnO4溶液除去乙烷中的乙烯气体杂质.
③只用水鉴别乙醇、甲苯、硝基苯.
④用如图装置检验溴乙烷与NaOH醇溶液共热发生消去反应.
⑤用盐酸洗涤盛放苯酚后的试管.
⑥检验溴乙烷中的溴元素:向NaOH溶液中先加几滴溴乙烷,加热,充分反应后,冷却,再加入AgNO3溶液,观察现象.
| A、②④⑤ | B、①③⑥ |
| C、①③ | D、②④⑥ |
下列关于物质的使用叙述不合理的是( )
| A、亚硝酸钠是常用的防腐剂 |
| B、婴儿食品可添加着色剂,以增加婴儿对食物的兴趣 |
| C、维生素C可防治坏血病,因而我们需要大量补充维生素C |
| D、药物可以帮助我们战胜疾病,但我们仍需合理用药 |
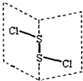 二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )
二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )A、S2Cl2的电子式: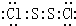 |
| B、S2Cl2为含有极性键和非极性键的非极性分子 |
| C、S2Br2与S2Cl2结构相似,熔沸点:S2Br2<S2Cl2 |
| D、S2Cl2与H2O反应化学方程式可能为:2 S2Cl2+2H2O=SO2↑+3S↓+4HCl |

 的所有原子
的所有原子